Mi a petefészekrák?
A petefészkek (ováriumok) páros belső női szaporító szervek, amelyek a kismedencében, a méh két oldalán helyezkednek el, és amelyek ivarsejteket (petesejteket) és hormonokat termelnek. A méhhez a széles méhszalag révén kapcsolódnak. A petefészkek teljesen csak a serdülőkorban, a menstruáció kezdetére fejlődnek ki. Egy petefészek 5-8 g súlyú, 2,5-5 cm hosszú, 0,5-3 cm széles, 0,6-1,2 cm vastag. A datolyához vagy a mandulához szokták hasonlítani. A petefészek állományának a felszínéhez közelebb eső részét kéregállománynak, középső részét velőállománynak nevezik.
A petefészkek petesejteket termelnek, amelyek a szaporodáshoz szükségesek. Emellett hormonokat is termelnek, amelyek sok egyéb hatás mellett a mellek növekedésére, a testalkat kialakulására és a menstruációs ciklus alakulására vannak hatással.
A petefészkekben előfordulhat jó- és rosszindulatú daganat is. A női kismedencei nemi szervek rosszindulatú daganatainak 25%-a indul ki a petefészekből, ezek nagy többsége, 90%-a a petefészek felszínét borító hámsejtekből ered (epithelialis eredetű adenocarcinoma). Más típusok kialakulhatnak a petesejtet képző csírasejtekből vagy a petefészket átszövő kötőszöveti sejtekből is.
Fejlett országokban a petefészekrák a nőgyógyászati daganatok tekintetében a méhtestrákkal holtversenyben a leggyakoribb, ugyanakkor a legtöbb halálos áldozatot követelő betegség. Hazánkban évente megközelítőleg 1300 új esetet diagnosztizálnak. Az esetek háromnegyedében már előrehaladott stádiumban kerül sor a diagnózisra. Ennek magyarázata, hogy korai stádiumban a betegség legtöbbször tünetmentes. Következménye, hogy agresszív kezelés ellenére is kedvezőtlen a betegség prognózisa.
Ezek a ráksejtek a petefészekből ugyanis könnyen, korán és gyorsan szétszóródhatnak, akár a vér- vagy nyirokáramon keresztül, vagy a hasüregben, az ascitesben (aszcitesz), vagyis a hasvízben, és áttéteket képezhetnek a hasüregben, a hashártyán, a környéki nyirokcsomókban, illetve távoli szervekben, leggyakrabban a tüdőben.
A petefészekrák felismerésekor a betegek átlagos életkora 65 év. Rosszindulatú petefészekdaganat ugyanakkor a fiatal, fertilis nőket is érintheti. A betegségnek nincsen konkrét okozója, azonban vannak hajlamosító tényezők, amelyek növelik a kialakulás kockázatát. Petefészekrák gyakrabban fordul elő például azoknál a nőknél, akik nem, vagy későn szültek, illetve akiknél a menstruáció korán, és/vagy a menopauza időszaka későn jelentkezett.
Genetikai tényezők is jelenthetnek a kialakulás szempontjából magasabb kockázatot: az összes petefészekrákos megbetegedés 10%-áért felelnek. Az öröklődő petefészekrák esetén a háttérben legtöbbször a BRCA1 és BRCA2 gén (Breast Cancer Antigen - Emlőrák Antigén) mutációja áll. Ezek a gének a DNS-hibák kijavításában játszanak fontos szerepet. A mutáció során azonban elvesztik azt a képességüket, hogy a külső (sugárzás, kémiai anyagok, stb.) vagy belső (szabálytalan sejtosztódás) okokból kialakuló károsodásokat kijavítsák a DNS-ben. Akinek a családjában halmozottan előfordul emlő- és petefészekrák, annak magasabb a kockázata a betegség kialakulására. Ma már lehetőség van onko-genetikai tanácsadás keretében a BRCA-gének vizsgálatára. Amennyiben igazolódik a mutáció, megelőző intézkedéseket lehet tenni a daganatos rizikó csökkentése érdekében.
Mint szinte minden betegségnél, a helytelen táplálkozás, az elhízás, a mozgásszegény életmód és dohányzás itt is növeli a kockázatot.
Vannak azonban olyan tényezők is, amelyek csökkentik a betegség kialakulásának kockázatát: a szoptatás és fogamzásgátló szedése például védő hatású a petefészekrákkal szemben.
A petefészek daganatai három nagy csoportba sorolhatók, melyeken belül számos szövettani típust különítünk el.
A petefészek daganatok lehetnek jó- és rosszindulatúak, ugyanakkor megkülönböztetünk egy átmeneti típust (borderline tumorok), melyek bár szövettanilag a rosszindulatúság jeleit mutatják, klinikai lefolyásuk igen kedvező.
A rosszindulatú daganatok szövettani típusa nagymértékben befolyásolja a kezelés módját.
A daganat agresszivitását jelző paraméter a grade.
A high grade daganatok agresszív viselkedésű, gyorsan osztódó, gyakran áttétet képező, ugyanakkor kemoterápiára legtöbbször igen érzékeny daganatok. A low grade daganatok sejtjei lassabban osztódnak, később adnak áttéteket, ezáltal a betegség lefolyása legtöbbször kedvezőbb, ugyanakkor a daganat sokkal kevéssé érzékeny a kemoterápiás kezelésre.
Újabban a daganatok molekuláris mintázatát is rutinszerűen vizsgálják, melynek további terápiás következménye lehet.
Hámeredetű daganatok
A petefészek rosszindulatú daganatainak leggyakoribb csoportja. Mai ismereteink szerint a petefészek felszíni hámjából, a méhkürt hámsejtjeiből és endometriosis szigetekből indulnak ki, ugyanakkor áttétek is lehetnek más szervek daganatai felől.
Számos szövettani típusa különíthető el, melyek gyakorisági sorrendben az alábbiak:
- High grade serosus adenocarcinoma
- Endometrioid adenocarcinoma
- Clear cell adenocarcinoma
- Low grade adenocarcinoma
- Mucinosus adenocarcinoma
- Áttéti daganatok (emlő, vastagbél, gyomor)
Sex-cord stromális tumorok
A petefészkek kötőszöveteiből kiinduló ritka daganatok, melyek fiatal és idős nőket egyaránt érinthetnek. Gyakran termelnek hormonokat (ösztrogén, tesztoszteron, stb.), ezáltal gyakran hormonális tünetek hívják fel a figyelmet jelenlétükre.
- Granulosa sejtes tumor
- Sertoli-Leydig sejtes tumor
Csírasejtes (germ cell) daganatok
Ritka daganattípus, mely leggyakrabban a fiatal nőket érinti. Gyorsan növekvő daganatok lévén, általában korai stádiumban tüneteket adnak.
- Dysgerminoma
- Éretlen teratoma
- Choriocarcinoma
- Yolk sack tumor
Szintén petefészekrák típusok:
- Rosszindulatú sex-cord stromális tumor
- Rosszindulatú csírasejtes daganat ( germ cell )
Tünetek
Korai stádiumban nincsenek (és később sem) specifikus tünetek, a méhnyakrákkal ellentétben nincsen rákmegelőző állapot, és nincsen olyan szűrőrendszer sem, ami felderítené a rosszindulatú elváltozást, ezért rendkívül nehéz időben felismerni a betegséget. A diagnózis legtöbbször már előrehaladott stádiumban születik meg, ekkor azonban a betegség prognózisa a széleskörű terápiás lehetőség ellenére rossz. A kezdeti tünetek hasonlítanak a gyomor- és bélrendszeri panaszok esetén jelentkező tünetekre. Ezért is nagyon fontos a következő szimptómák tartós fennállása esetén orvoshoz fordulni:
- hasi puffadás, diszkomfort
- étkezéskor szokatlanul korán bekövetkező teltségérzés
- gyomorégés
- emésztési zavarok
- hasi és/vagy deréktáji fájdalom
- vizelési/székelési panaszok
- fogyás
- haskörfogat növekedés
- nehézlégzés
Nagyobb a valószínűsége, hogy ezek a tünetek a petefészekrákot jelzik, ha
- újonnan, egy éven belül jelentkeztek
- gyakran, egy hónapon belül akár 12 napon át is előfordulnak.
Tünetek esetén fordulj háziorvoshoz vagy nőgyógyászhoz ( szakrendelő/magánrendelő)!
Amennyiben a tünetek nem múlnak, és háziorvost keresel fel, ragaszkodj hozzá, hogy kizárja a petefészekrák valószínűségét!
A Mályvavirág Alapítvány segít az orvos és intézmény megtalálásában.
Mályvavirág Szakmai Bizottság
A Mályvavirág Alapítvány szorosan együttműködik egészségügyi szakemberekkel - legyen szó akár egy kiadvány elkészítéséről, diagnózis felállításáról, vagy műtétekről, terápiákról, másodvéleményről, intézményi együttműködésről, felvilágosító munkáról, információ szerzésről vagy átadásról.
Keresd bizalommal őket!
https://malyvavirag.hu/szakmai-bizottsag
Onkológiai Centrumok, melyekkel a Mályvavirág Alapítvány együtt dolgozik:
Budapest
- Országos Onkológiai Központ: https://onkol.hu/
- SOTE/Semmelweis Egyetem Radiológiai és Onkoterápiás Klinika: https://semmelweis.hu/klinikaikozpont/
- Dél Pesti Centrumkórház, Egyesített Szent László és Szent István Kórház
- https://www.dpckorhaz.hu/osztalyok/betegellatast-vegzo-osztalyok/szuleszet-nogyogyaszati-nogyogyaszati-onkologiai-osztaly/
Debrecen
- Debreceni Egyetem Klinikai Központ Szülészeti és Nőgyógyászati Klinika: https://noiklinika.unideb.hu/
A linkek eléréséhez kattints a címekre!
A petefészekrákról/Rákgyógyítás.hu
Kivizsgálás / Diagnózis
A sokat ismertetett tünetek esetén nagyon fontos a nőgyógyászati vizsgálat. Petefészekrák esetén a fizikális vizsgálat és már maga a páciens megtekintése is informatív.
A petefészek anatómiai elhelyezkedése miatt a petefészekből (és petevezetékből) kiinduló daganatoknak van elegendő helyük a növekedésre, ezért korai stádiumban általában nem okoznak panaszokat. A betegség az esetek ¾ részében akkor kerül felismerésre, mikorra már szétszóródnak a daganatos sejtek a szervezetben, és ez panaszokat okoz.
Jellemző tünetek: haskörfogat növekedése, teltségérzés, tartós alhasi fájdalom, gyakori vizelési inger.
Ha a panaszok hátterében felmerül a petefészekrák gyanúja, a betegség igazolására és kiterjedtségének felmérésére különböző vizsgálatokra lehet szükség.
-
Kórtörténet részletes kikérdezése, érintve a családban előforduló daganatos megbetegedéseket.
-
Nőgyógyászati tapintásos vizsgálat során a belső női nemi szervek nagyságát, elhelyezkedését, a daganat környező szervekhez és a medencefalhoz való viszonyát, valamint a hashártya érintettséget lehet közelítőleg felmérni. Tükörvizsgálattal a hüvely és a méhszáj vizsgálható. A növekvő petefészekdaganat a petefészek megnagyobbodását eredményezi, a megnagyobbodott petefészek pedig jól tapintható. Azonban a megnagyobbodott petefészkek tapintása nem jelent petefészekrákot, mivel a jóindulatú daganatok (melyek a petefészkek daganatainak 80%-át teszik ki) is okozhatják a méret növekedését, megnagyobbodáshoz vezethetnek.
Ritkán egyidejűleg végzett hüvelyi és végbél-vizsgálatra is szükség van.

Az ultrahangos vizsgálatnak két fajtája van: hüvelyi és hasi ultrahang. A készülék által kibocsátott hanghullámok visszaverődése által képződik a kép a vizsgált területről, amely mutatja a méh, a petevezetékek, a petefészkek és a környező szövetek állapotát.
-
Hüvelyi ultrahang vizsgálat során a hüvelybe vezetett ultrahangos szonda segítségével lehet képet kapni a belső nemi szervekről és a daganat nagyságáról, érellátásáról valamint annak közvetlen környezetéről.
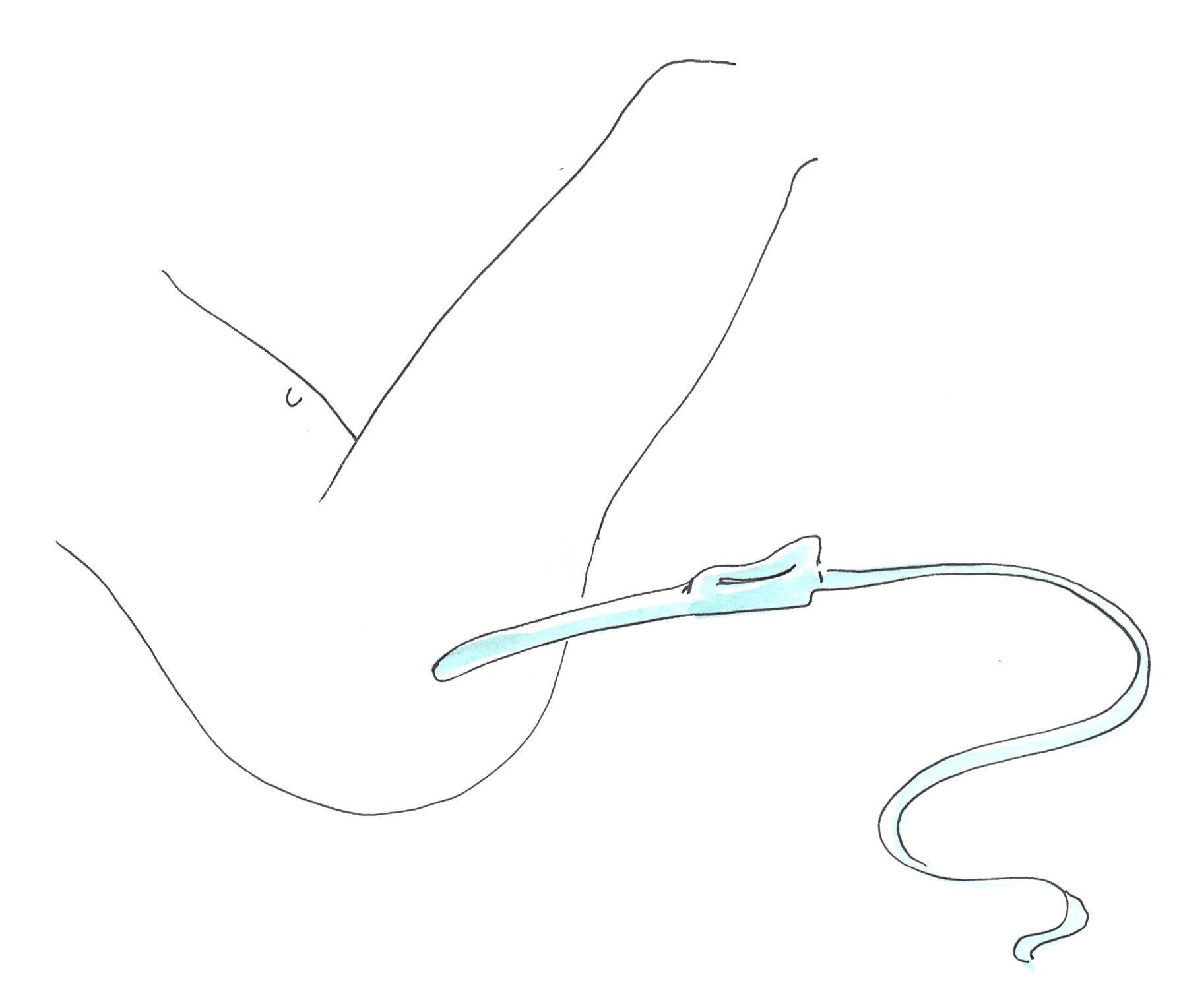
A vizsgálat nem jár sugárterheléssel, és általában fájdalommentesen kivitelezhető.
-
Hasi ultrahang vizsgálat során a hasfalon keresztül az összes hasi szerv vizsgálható. Segítségével megállapítható, hogy a daganat a hasüregen belül mekkora kiterjedésű, vannak-e nagyobb áttétek vagy hasi folyadék (ascites). A vizsgálatot a hasfalra kent kontakt gél segítségével végzik.
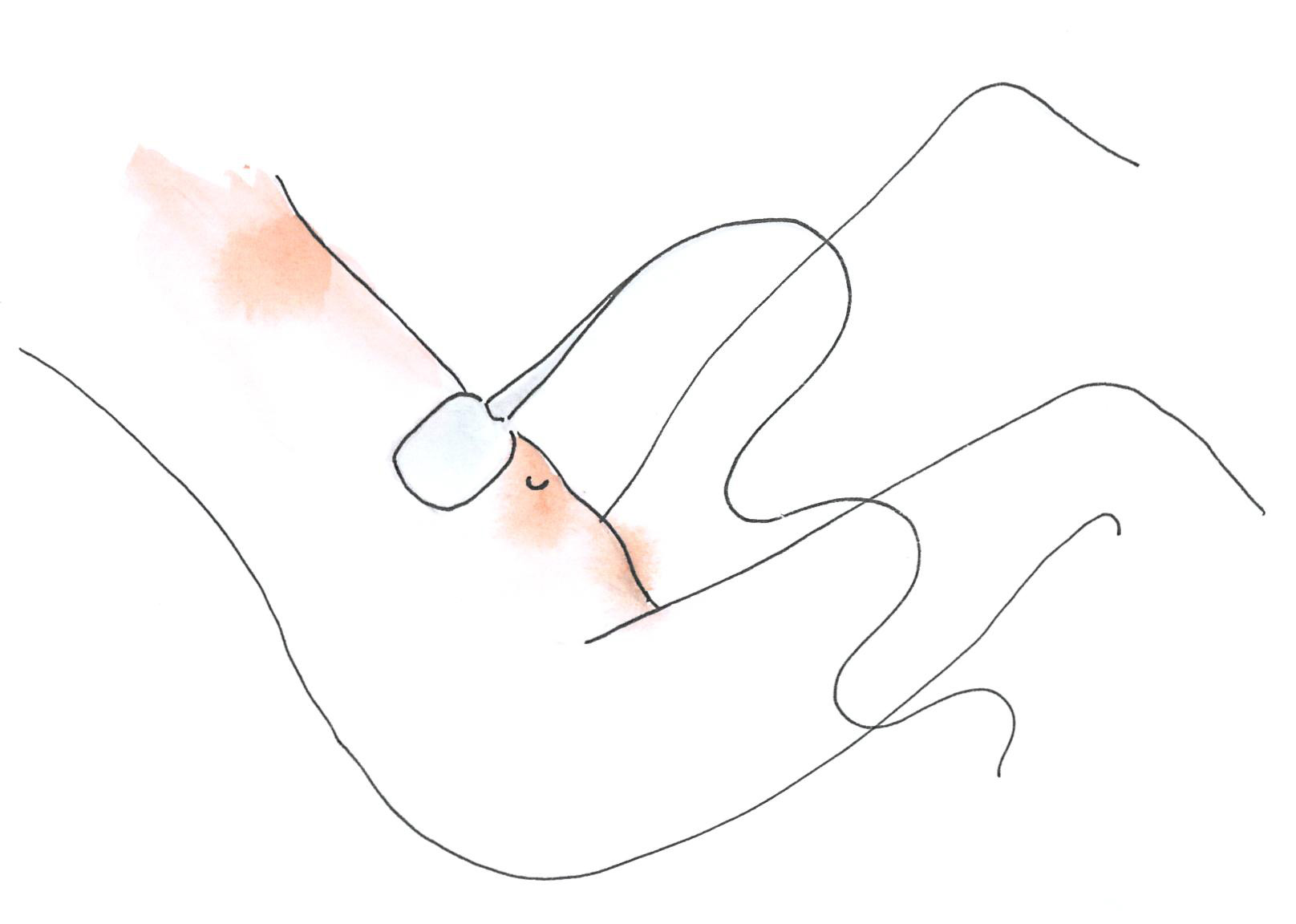
-
Mellkas röntgen segítségével a mellüregi folyadékképződést lehet kizárni vagy megerősíteni.
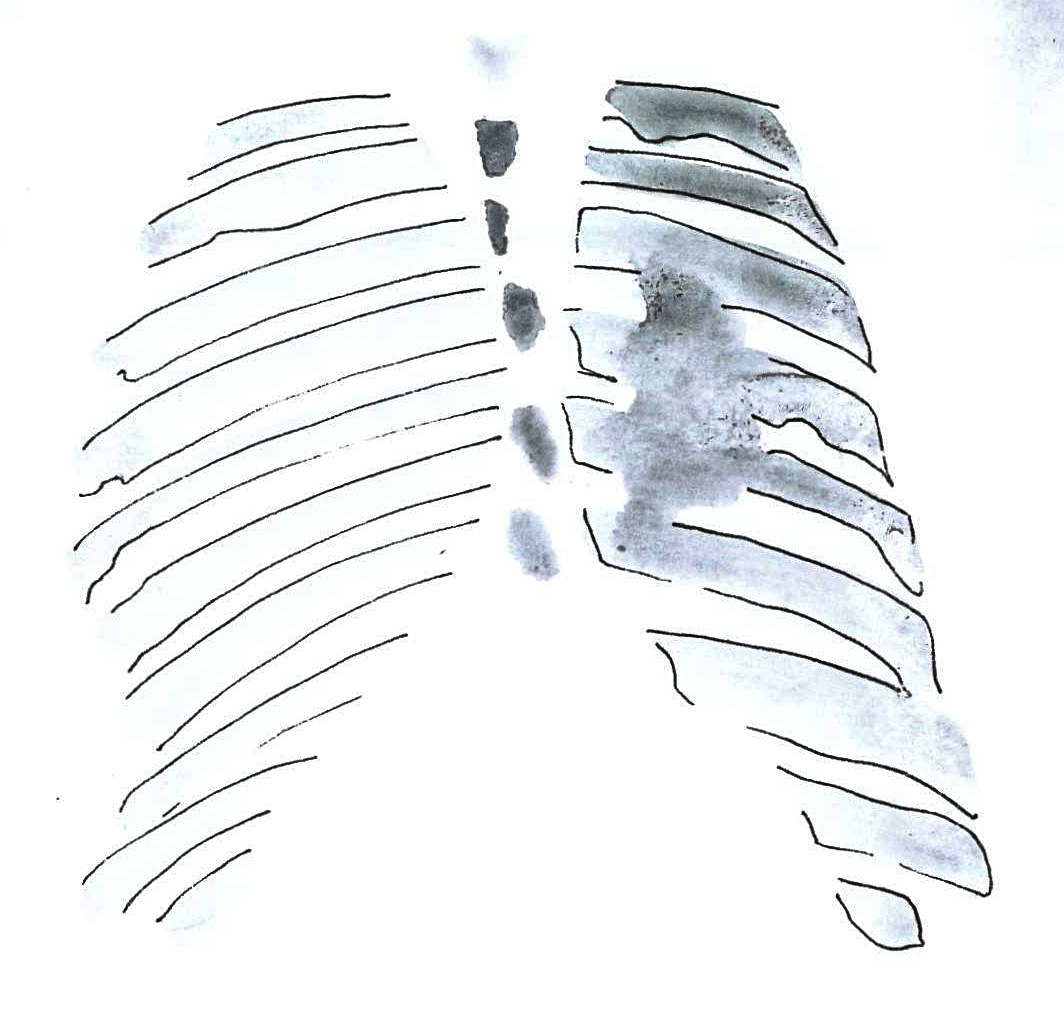
-
Vérvétel során a vérképen, ionszinteken, vese- és májfunkciós értékek vizsgálatán kívül speciális tumormarkerek (CA-125, HE4 ) szintje is megállapításra kerül. Ezek segítenek a daganat gyanújának megerősítésében, a terápia hatékonyságának felmérésében, és a kezeléseket követően a daganat kiújulásának időben történő felismerésében.
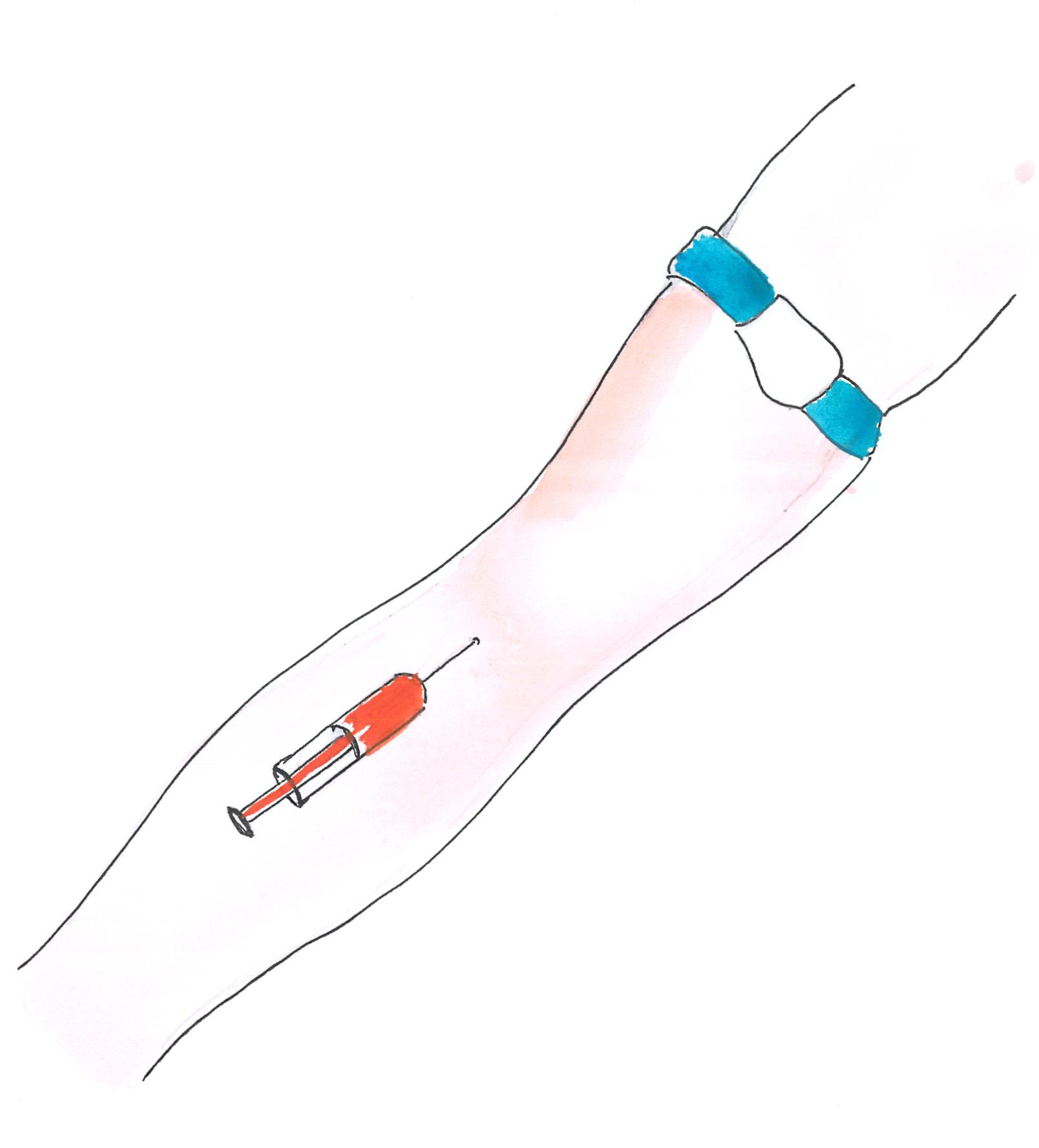
-
A hasi folyadékból történő diagnosztikus mintavétel során daganatos sejtekhez lehet jutni, melyek vizsgálatával meg lehet erősíteni a diagnózist. A nagy mennyiségű ascites terápiás célú punkciója a beteg panaszait jelentősen csökkenteni tudja. A beavatkozás helyi érzéstelenítésben történik.
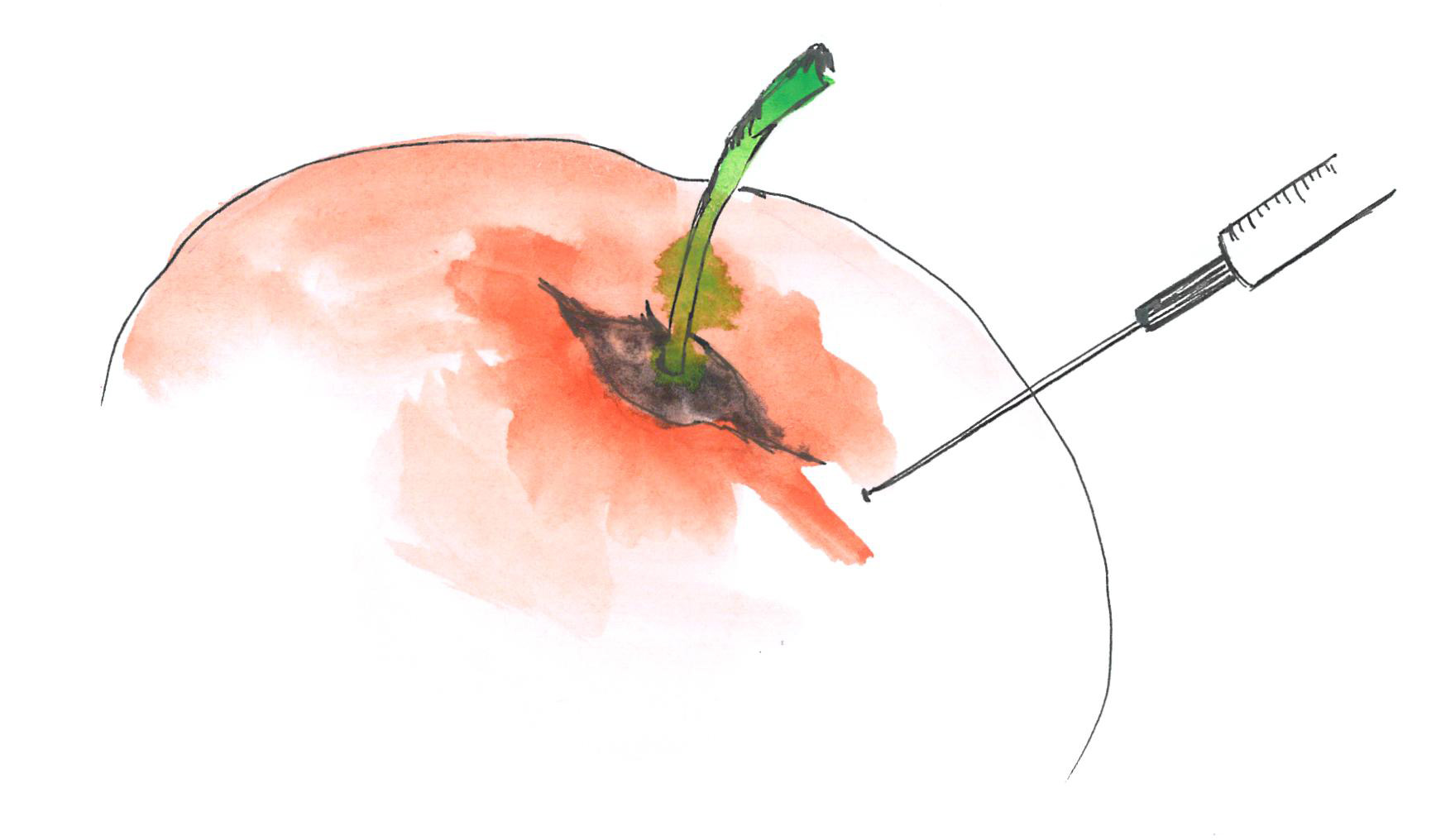
-
Képalkotó vizsgálatok: Képalkotó vizsgálatokkal megállapítható, hogy kialakult-e elváltozás a petefészken belül, és ha igen, akkor hol, mekkora a mérete, milyen az alakja. CT és MR segítségével a daganat helyi kiterjedtségét és a távoli áttétek jelenlétét lehet megállapítani, mely a terápia tervezésében és a terápia hatékonyságának nyomon követésében alapvető fontosságú. PET CT vizsgálat, bár érzékenyen, kimutatja a petefészekdaganatot, de ebben a daganattípusban hazánkban nem finanszírozott. Amennyiben a vesefunkciók rendben vannak, az MR és a CT vizsgálat előtt kontraszt folyadékot kell fogyasztani, amely elősegíti a tisztább kép alkotását. A vizsgálat során háton kell feküdni, a vizsgálóasztal egy alagút-szerű gépben mozog, melynek folyamán a gép felvételeket készít minden irányból, amely később egy részletes képpé áll össze számítógép segítségével.
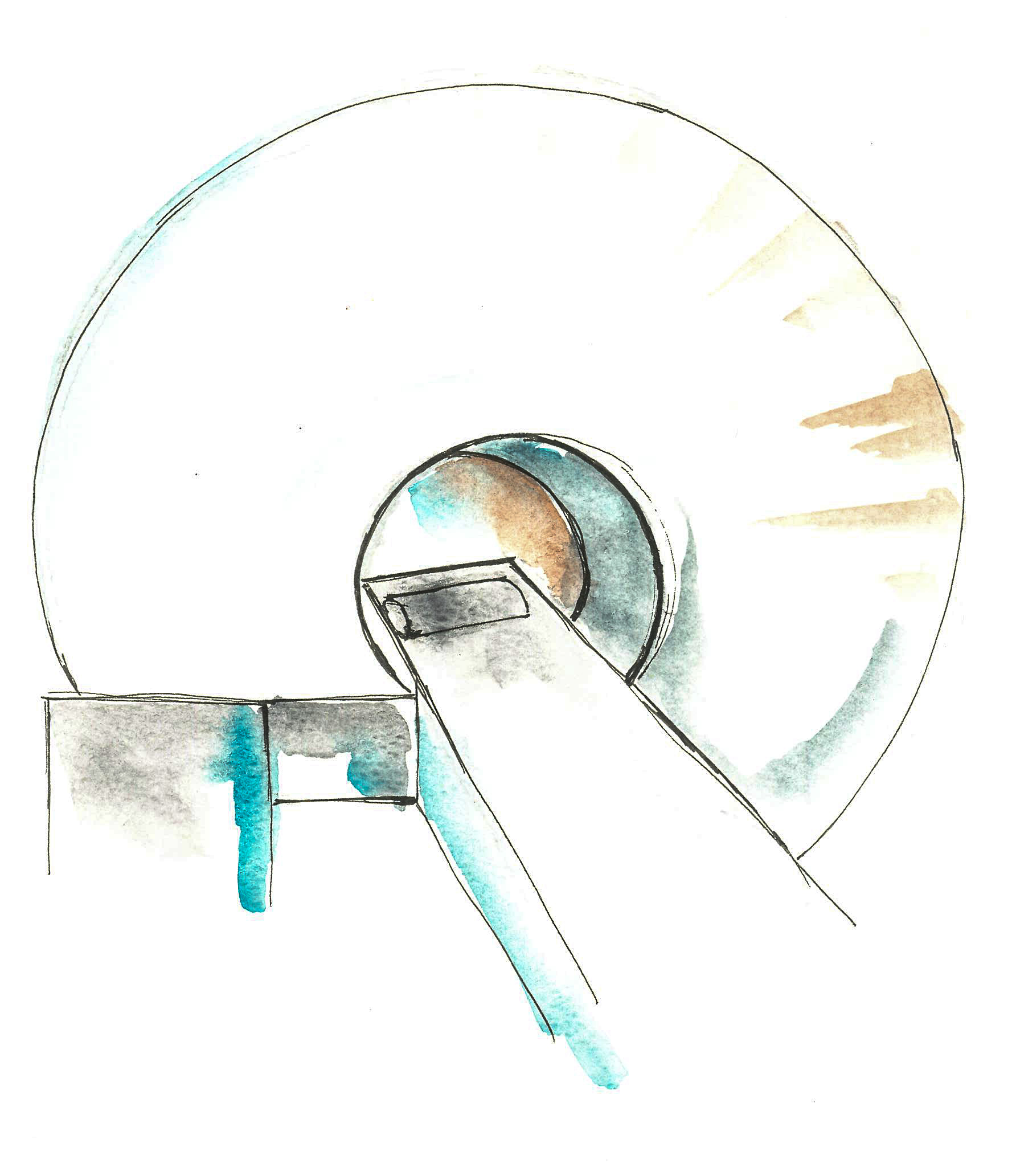
-
Colonoscopia (béltükrözés), és cystoscopia (hólyagtükrözés) segítségével a vastagbélre és a húgyhólyagra való daganatos ráterjedést lehet megállapítani, melynek ismerete a műtéti ellátás során fontos lehet. A vizsgálatokat bódítás alatt, illetve helyi érzéstelenítésben, megfelelő előkészítést követően végzik. A vizsgálat során egy csövet vagy katétert vezetnek a végbélbe vagy a húgyhólyagba.
Az esetek nagy részében a petefészekrák diagnózisát műtét során lehet felállítani, mely beavatkozás egyben terápiás célú is, hiszen így a daganat egyben eltávolításra is kerül. Fontos tudni, hogy a petefészek elváltozások többsége jóindulatú, amely a műtétet követően nem igényel további kezelést.
Az ultrahang vizsgálat segítségével mintavétel is történhet. Ez az ún. core-biopszia, mely az elváltozásból történő mintavétel, vagy hüvelyen, vagy hasfalon keresztül egy hosszú, tűszerű eszközzel. Bár a leírás és maga az eszköz ijesztőnek tűnhet, a páciensek elmondása alapján, legtöbb esetben csak egy pillanatnyi fájdalmat okoz a mintavétel. Ezt a vizsgálatot nem minden kolléga végzi el, néhány helyen van csak lehetőség egyelőre core-biopszia vételére. A mintát ezt követően szövettani vizsgálatra küldik, és szövettani diagnózishoz juthatunk pár napon belül.
A petefészekrák kivizsgálását és a diagnózis megszületését követően a daganat kezelésében jártas szakemberek - onkológiai szakbizottság, az onkoteam tagjai - közösen tesznek javaslatot az egyénre szabott kezelésre.
Amennyiben a képalkotó alapján daganatmentesség a műtéttel nem érhető el, akkor kemoterápiával kezdődik a kezelés. Ez esetben neoadjuváns kemoterápiának nevezzük a kezelést. Elsősorban ebben az esetben van jelentősége a core-biopsziának, hiszen a szövettani típusnak megfelelő kemoterápiás kezelést kell kezdeni, mint neoadjuváns kezelés. 3-4 kemoterápiát követően (3 hetente történik kezelés) ismét képalkotó vizsgálatot végeznek, és amennyiben ez alapján a folyamat kiterjedése csökkent, daganatmentesre operálható a páciens, akkor műtét következik. Ezt intervallum műtétnek nevezzük, mely arra utal, hogy a kemoterápiás kezelés ciklusai között történik a beavatkozás, vagyis a műtétet követően a kemoterápiát folytatni kell (további 3 kezelés).
Tumormarkerek
- CA125
- HE-4
ROMA score: a hámeredetű petefészekrákok valószínűsítését támogatja. Ez egy algoritmus.
- OVA1 (CA125, béta-mikroglobulin, apolipoprotein A1, prealbumin, transferrin)
- HE4 (Human epididymis protein)
- Beteg menopauzális státuszának figyelembe vétele
Folyadékbiopszia (petefészekrák sejtek vérből való kimutatása)
Képalkotó vizsgálatok
- UH
- CT - ascites (hasvíz), retroperitonealis (hashártya mögötti), limfadenopátia (nyirokmirigy), peritoneális (hashártya) karcinózis kimutatásra
- MR - szerven belüli lágyrészek
Mi az a patológia? Ki az a patológus?
A patológia a legszerteágazóbb és így a legizgalmasabb szakterülete az orvostudománynak.
A patológia 85%-ban az betegből eltávolított szövet- és sejtminták feldolgozását végzi diagnosztikus céllal. A hatályos Egészségügyi törvény (1997. évi CLIV. tv. 204§) szerint valamennyi szövet, szerv vagy szervrészlet esetén szövettani vizsgálatot kell végezni. A vizsgálatot a patológiai laboratórium végzi, mely minden kórházban, egyetemen és országos intézetben működik. Vannak magánlaboratóriumok is.
A patológiai laboratóriumokban speciális személyzet dolgozik. Patológus szakorvosok, szakorvos jelöltek, rezidensek, biológusok mellett magasan képzett szövettani-, immunhisztokémiai szakasszisztensek, citológus előszűrő asszisztensek, okleveles boncmesterek, adminisztratív munkatársak, logisztikai segítők végzik napi rutin szerint feladataikat.
A patológus az orvosi egyetem elvégzését követően 5 év után szakvizsgát tesz szövettanból és kórbonctanból. Kiegészítő szakvizsga a citopatológia és a molekuláris genetikai diagnosztika. A patológus minden szakiránnyal foglalkozik, de hosszú évek alatt specializálódhat például többek között nőgyógyászati daganatok és betegségek diagnosztikájára is. A patológus az onkoteam meghatározó tagja.
A szövettani mintát a klinikus orvos veszi le, majd ezt a szövetdarabot előírás szerint a patológiai laboratóriumba küldi, ahol ezt feldolgozzák. A szövettani vizsgálat speciális tudást igényel, sok évi gyakorlás és tapasztalat szükséges hozzá. A szakmai előírásokat minden laboratórium egységesen alkalmazza. Például méhnyakrák-diagnosztikában meghatározott szövetblokkokat vizsgálnak, nyirokcsomókat elemeznek, és immunhisztokémiai vizsgálatokat végeznek.
A vizsgálatról meghatározott tartalmú részletes szövettani lelet készül, a szövettani diagnózis alapján tervezhető meg a beteg további kezelése. Amennyiben a kezelési tervhez szükséges, molekuláris genetikai diagnosztikus vizsgálatokat végeznek. Centrumlaborokban sokgénes vizsgálatokat, genomikai profilozást is végeznek közfinanszírozottan.
A konvencionális vagy liquid-based méhnyak kenetek, testüregi folyadékok, vékonytűvel vett aspirátumok vizsgálatát a citopatológus végzi. A vékonytű-aspirátumot klinikus orvos és a citológia szakrendelőben maga a citopatológus is leveheti.
A patológus sokat foglalkozik a betegekkel, gyakran hosszas nyomozómunkát folytat a beteg érdekében, hogy a legpontosabb diagnózis születhessen. A patológus részleteket, összefüggéseket vizsgál, leletével segíti a klinikus gondolkozását. A patológia a háttérben dolgozik, a betegek most már sokkal többet tudnak a szövettani- vagy citológiai leletük jelentőségéről. Ezek a leletek az EESZT Lakossági Portálról letölthetők.
Stádiumok
A stádium meghatározásában a folyamat lokális kiterjedése, távoli áttétei, illetve a nyirokcsomó státusz a meghatározó.
I. stádium esetén a folyamat a petefészekre/petefészkekre vagy petevezetőre/petevezetőkre lokalizált.
IA: A daganat tokon belüli és csak az egyik petefészket érinti.
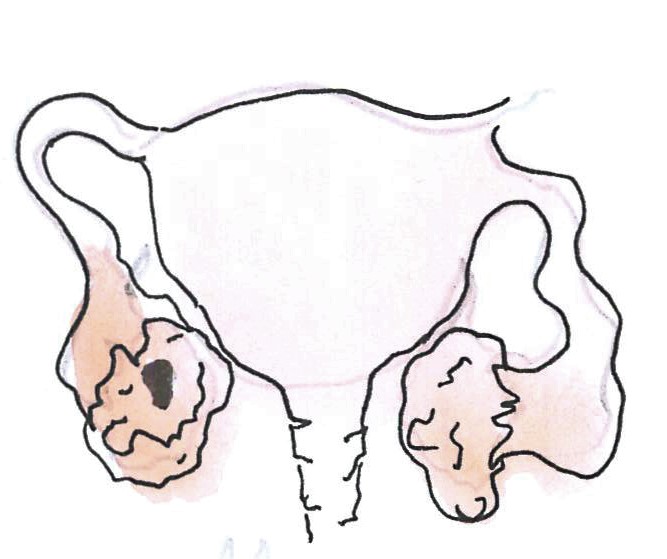
IB: A tokon belüli daganat mindkét petefészket érinti.
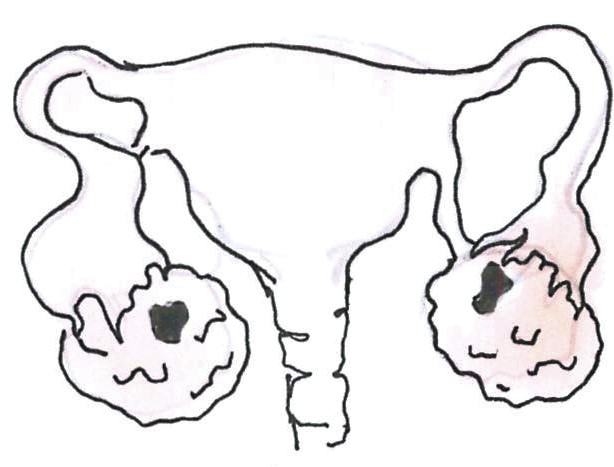
IC: A daganat a tokot áttörte, vagy a tok megrepedt, a hasüregben folyadék képződhet (ascites).
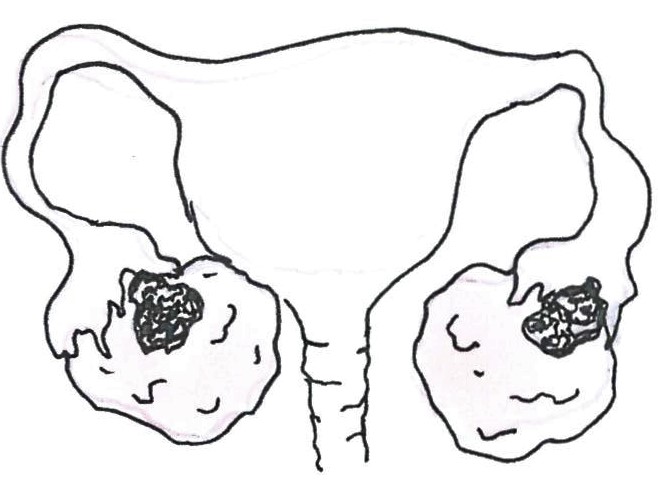
II. stádiumban a betegség a petefészkekre/petevezetőkre, illetve a kismedence szintjét meg nem haladó szervekre lokalizált (pl. méh).
IIA: A daganat átterjedt a méhre vagy a méhkürtre.
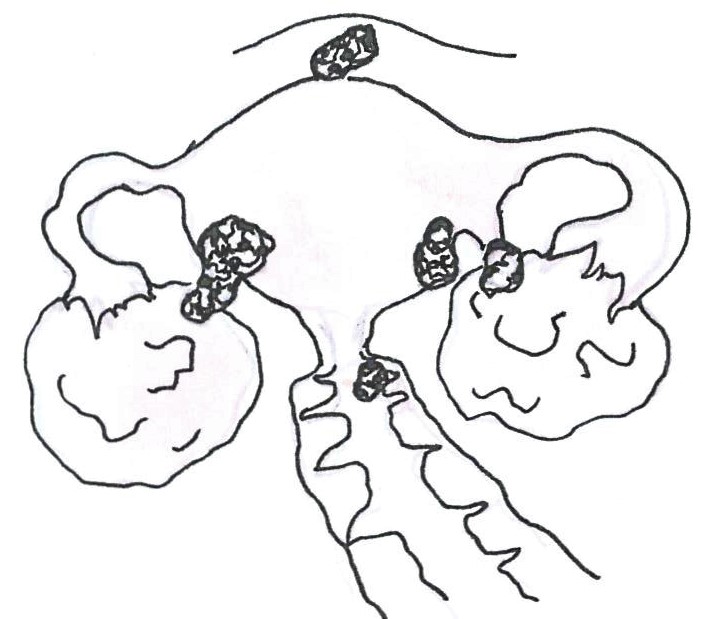
IIB: A daganat egyéb kismedencei szerveket is érint.
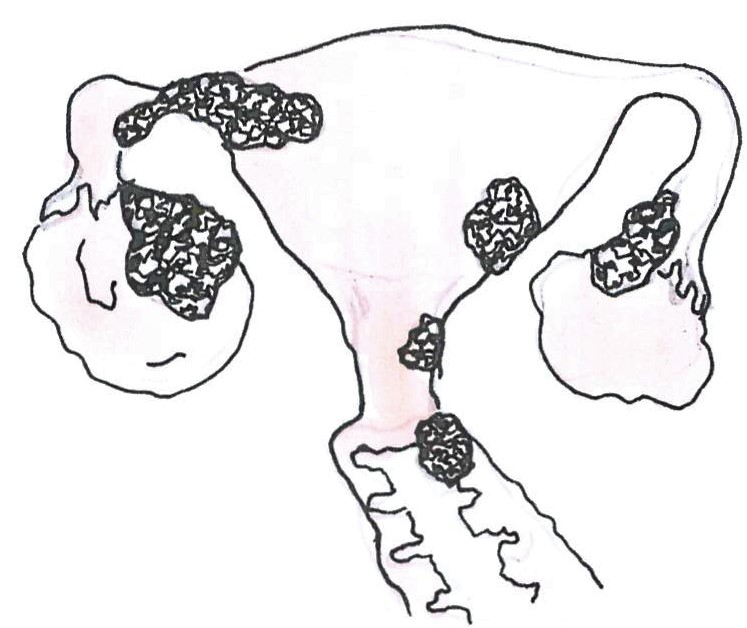
III. stádiumban a daganat a kismedencei szerveken túl áttétet ad a kismedence feletti hashártyára vagy a nagyerek melletti nyirokcsomókba.
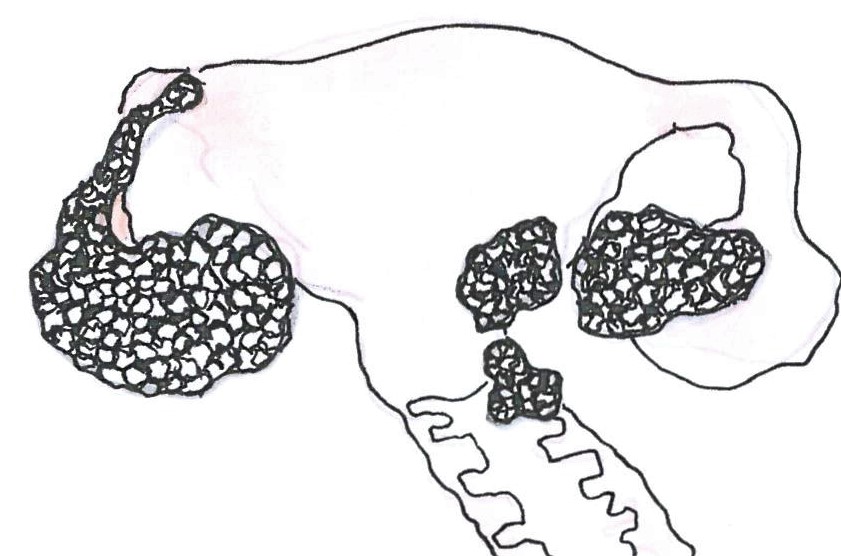
IIIA: A daganat nyirokcsomó áttétet képez.
IIIA1: Nyirokcsomó áttétet képez, vagy
IIIA2: mikroszkópos áttétek találhatóak a hashártyán kismedencén kívül a nyirokcsomóáttét mellett.
IIIB: 2 cm-nél kisebb hashártyaáttétek a hashártyán a kismedencén kívül
IIIC: 2 cm-nél nagyobb hashártyaáttétek a hashártyán a kismedencén kívül
IV. stádiumban a betegség tumort okoz az egyik, vagy mindkét petefészekben, és távoli áttéteket képez, a májban és/vagy a lépben is jelen van, a beleket is érintheti, illetve hasüregen kívül is megjelenik pl. mellhártyán vagy lágyékhajlati nyirokcsomókban.
IVA: mellhártya érintettség van, pozitív citológiai lelettel, távoli szervi áttét hiányában.
IVB: távoli szervi áttét van.
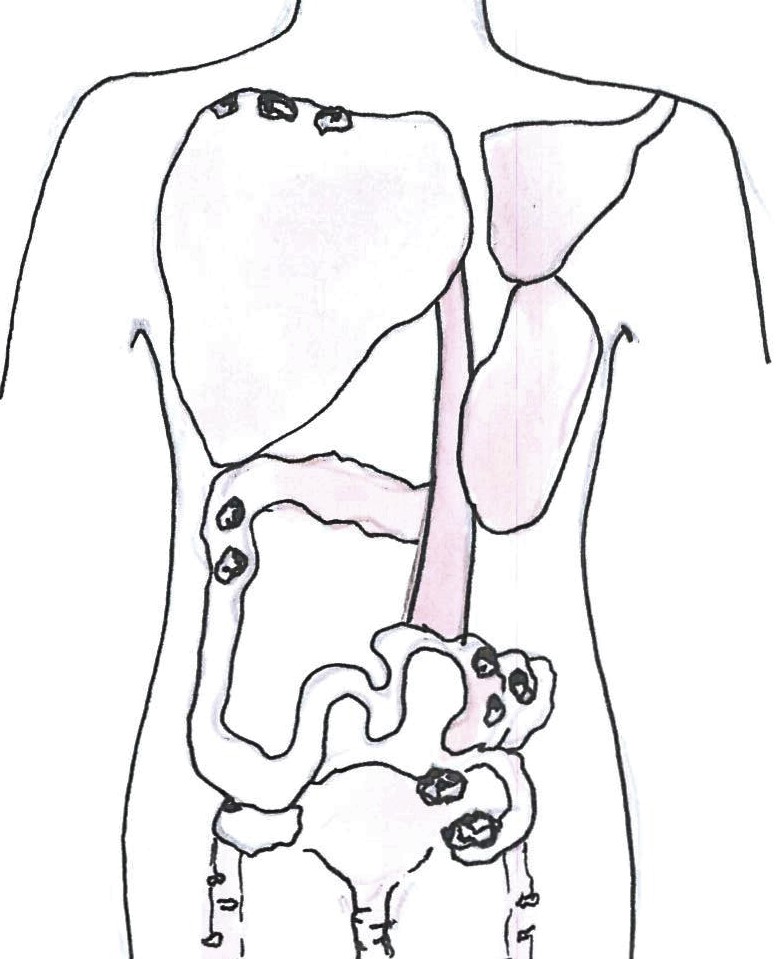
Szövettan tekintetében több csoportot különíthetünk el, amelyek alapvetően meghatározzák a kezelés módját. Adott szövettan dönti el, hogy nyirokcsomó-eltávolítás milyen magasságig indokolt, vagy, hogy a vakbelet például ki kell-e venni. Ugyanígy a szövettani típus határozza meg a kemoterápia fajtáját is, és következtethetünk a betegség lefolyására is akár.
FONTOS:
A nőgyógyászati daganatok kezelése onkológiai centrumban történjen, erre a területre specializálódott nőgyógyász onkológus, klinikai onkológus, daganatsebész által!
GÉNVIZSGÁLAT
Molekuláris patológiai vizsgálat
Ezek olyan vizsgálatok, amelyek előre jelezhetik, hogy az adott daganatra milyen gyógyszer lehet hatásos. Azt vizsgálják, hogy van-e mutáció a génekben, ha igen, akkor ezek meghatározásra kerülnek, majd az eredmények függvényében megállapítható, hogy van-e olyan kezelés, ami a betegnek segíthet a gyógyulásban, vagy az élet meghosszabbításban. Szekvenálásnak hívjuk a daganatsejtek felépítésének, mutációinak kimutatását, a daganatsejtek elemzését. Nagyon költséges eljárás. Fontos hangsúlyozni, hogy azokat a molekuláris génvizsgálatotokat, melyek a kezelést befolyásolják, vagy amelyek jelenlétében van gyógyszeres kezelési lehetőség, specializált daganatközpontban, államilag finanszírozva is el lehet érni.
Géntérkép
Az emberi géntérkép elkészítése áttörést hozott az orvostudományban. Azon túl, hogy megismertük az emberi genomot, új utakat nyitott meg a betegségek genetikai eredetének feltérképezésére. Ma már nem csak ritka genetikai betegségeket lehet vizsgálni ezekkel a módszerekkel, géntérképünk többek között azt is megmutatja, hogy hordozunk-e olyan mutációkat, amelyek betegségeket okoznak, illetve, hogy van-e olyan eltérés, amely segít a betegség kezelésében. Sajnos kevesebb a terápia, mint a kimutatott mutációk, de a teljes géntérkép megismerése segíti a tudomány fejlődését, új lehetőségek feltárását, rengeteg adatot szolgáltat.
A teljes géntérkép elkészítése nagyon költséges, és csak kivételes esetben támogatja a biztosító. A daganatos betegségek diagnosztikájában ugyanakkor egyre nagyobb szerepet kapnak a molekuláris genetikai vizsgálatok, amelyek a daganat jellemzőinek részletes feltérképezése révén hatékony, egyénre szabott kezelést tesznek lehetővé. Fontos hangsúlyozni, hogy azokat a molekuláris génvizsgálatotokat, melyek a kezelést befolyásolják, vagy amelyek jelenlétében van gyógyszeres kezelési lehetőség, specializált daganatközpontban államilag finanszírozva is el lehet érni.
BRCA
A BRCA a Breast Cancer Antigen angol rövidítése. Elsőként az emlőrák kapcsán ismerték fel ezt a gént, innen jött az elnevezés. Ezek a gének minden emberben megtalálhatóak.
A BRCA1 és BRCA2 gének olyan fehérjéket kódolnak, amelyeknek az a feladata, hogy segítsenek a sejtben létrejövő DNS-károsodások javításában, és így biztosítsák a sejtek normális működését. Előfordul, hogy valamelyik BRCA gén működése meghibásodik (ezt nevezzük mutációnak), emiatt a DNS-hibajavítás nem működik megfelelően, ami daganatképződéshez vezethet. A mutáció megjelenhet csak a daganatszövetben – ez nem öröklődik, vagy a test valamennyi sejtjében - ilyenkor örökletes BRCA mutációról beszélünk.
Ez a mutáns gén generációkon keresztül öröklődhet, és elsősorban az emlőrák és a petefészekrák kialakulására hajlamosít, de egyéb daganattípusokban is szerepet játszik, pl. prosztatarák, hasnyálmirigyrák.
Fontos tudni, hogy nem minden petefészekrák, illetve emlőrák hátterében áll BRCA-mutáció.
BRCA jelentősége
-
Ha a családban halmozottan fordult elő emlőrák, petefészekrák, hasnyálmirigy- vagy prosztatarák, különösen fiatal korban, akkor érdemes megnézetni a BRCA-mutációt, mert ez öröklődhet. A vizsgálat vérből történik, és genetikai tanácsadás előzi meg. Ha igazolódik a mutáció, szakorvosi konzultációt folytatnak le, hogy az emlő- és petefészekrák kialakulásának kockázatát csökkenteni tudják, illetve időben felismerjék, ha daganat alakul ki. Erre térítésmentesen az Országos Onkológiai Intézetben (Budapest), a Semmelweis Egyetemen (Budapest), a SZTE Klinikai Központban (Szeged) van lehetőség. Ezek mellett magánúton is elérhető a tanácsadás és a BRCA-tesztelés.
-
Ha már kialakult a petefészekrák, a terápiaválasztás miatt fontos tudni, hogy fennáll-e a BRCA-mutáció, mert befolyásolja a terápiát, új lehetőségeket nyit meg. Személyre szabott terápia, ún. fenntartó terápia adható a BRCA 1, 2 mutáció-pozitív betegeknek. Ilyenkor a daganatból célszerű elvégezni a vizsgálatot, erre több intézetben van lehetőség. Ezt a kezelőorvos (onkológus) kérheti meg.
HRD - Homologous recombination deficiency, homológ rekombinációs deficiencia
A DNS-hibajavítás a sejtekben állandóan zajló folyamat, amely elengedhetetlen a túléléshez. DNS-károsodást okozhatnak az anyagcsere-folyamatokból származó melléktermékek (reaktív oxigéngyökök) és külső környezeti tényezők, például UV-sugarak, egyéb sugárzás, szintetikus vegyszerek, toxinok stb., aminek következtében naponta több százezer molekuláris károsodás alakul ki egy-egy sejtben. Ezek a károsodások roncsolják a DNS szerkezetét, így megváltoztathatják a génekben kódolt információk olvasását, a javításukra szolgáló mechanizmusok folyamatosan működnek. A DNS kettős spirálszerkezetét ért károsodás típusától függően többféle javítási stratégia létezik.
Amikor a kromoszóma két szála közül csak az egyik hibás, a másik szál használható mintaként, ami alapján megtörténhet a károsodott szál javítása. Az egyszálú törések javítására szolgálnak például a kivágó mechanizmusok, amelyek eltávolítják a károsodott nukleotidot (a DNS építő egysége), és a helyére egy sértetlent építenek be úgy, hogy a másik DNS szál nukleotidját kiegészítse. Ilyen a báziskivágó javítás, amely egyetlen károsodott nukleotidot javít ki. A nukleotidkivágó javítás 2‒30 nukleotid hosszúságú károsodott szakaszokat, az össze nem illő párokat javítja ki (mismatch repair), illetve a DNS megkettőződése és az azt követő rekombináció során keletkező hibás nukleotidpárokat is kijavítja.
Kettősszálú törés esetén a javítás két fontos mechanizmusa: a nem homológ végek összekapcsolása, illetve az ún. homológ rekombinációs javítás. A rekombinációs javító mechanizmus túlnyomórészt a sejtciklus azon fázisaiban működik, amelyekben a DNS megkettőződik, vagy már megkettőződött. Az emberi genomban sok gén több példányban van jelen, így az azonos szekvenciák (gének sorrendje) több forrásból elérhetők. Az ilyen másolatokra hagyatkozó rekombinációs javítás azonban kromoszomális átrendeződésekhez vezet.
A „nem homológ végek összekapcsolása” során a törés két vége szekvencia-minta nélkül kapcsolódik össze, gyakran DNS-szekvenciák vesznek el, így ez a javítás mutációt is okozhat.
Vannak, akiknek a szervezete nem tudja kijavítani azokat a hibákat, amelyek a DNS-ükben jelennek meg, amikor új sejteket hoznak létre. Ezt homológ rekombinációs hiánynak (HRD) nevezik.
A daganatos sejtekben, amelyekben hiányoznak a hatékony homológ rekombinációs javítás alapvető funkcionális összetevői, mint például a BRCA1/2, vagy az egyéb, úgynevezett HRR-ben (homológ rekombinációs repair-ben, vagyis javításban) szerepet játszó gének, a DNS kettős spirál törések nem tudnak pontosan vagy hatékonyan kijavítódni, ami jelentős homológ rekombináció hiányhoz (HRD: homológ rekombinációs deficiencia) vezet. Ilyenkor az alternatív és „hibahalmozó” útvonalak aktiválódnak, mint például a „nem homológ vég-a-véghez illesztés”, ami a genom nagyfokú instabilitáshoz vezet. A DNS megkettőződési ciklusok során ez az instabilitás fokozódik.
A HRD (homológ rekombinációs deficiencia) és a kialakuló genom-instabilitás különböző elváltozások ill. nagy átrendeződések formájában jelenik meg a kromoszómán. Ezen elváltozások, az ún. genomikai „hegek” kimutathatóak, és ezek alapján, meghatározott kritériumok szerint egy összetett pontszám számolható ki. Bizonyos HRD-pontszámok magában foglalják a BRCA1/2 gének mutációját és/vagy a genomikai instabilitást, így egy határérték segítségével megállapítható a HRD-pozitivitás. A BRCA- illetve a HRD-státusz, valamint a platina-érzékenység (platina-alapú kemoterápiára adott megfelelő válasz) fontos előrejelző tényezője a petefészekrák fenntartó kezelésében alkalmazott ún. PARP-inhibitorok hatásosságának.
Mályvavirágok Közössége a Facebookon - titkos és zárt csoport:
Nőgyógyászati daganattal érintettek csoportja. A tagok beszélgetnek, információkat osztanak meg, kérdeznek, tanácsolnak, segítik egymást. A csoportban szakemberek is jelen vannak, moderált, szabályzattal ellátott közösség a Facebookon.
Itt mindenről szó van, jó és rossz dolgokról is. Lehet aktívan részt venni benne és hátulról figyelni. Ki lehet menni bármikor és újra kérni a felvételt.
Titkos és zárt, nem látszik az adatlapon, ha csatlakozol, és megtalálni sem lehet.
Csoportba bejutás:
1. lépés, hogy like-old a Mályvavirág nyílt oldalt, ha még nem tetted meg,- csak így tudunk a zárt csoportba tenni.
2. lépés: kérjük töltsd ki ezt a kérdőívet: https://forms.gle/uvf6tasEVrpf7j4K6
3. lépés: Facebook értesítés érkezik neked, hogy bejöhetsz a csoportba.
Amennyiben elakadnál, kérjük, vedd fel velünk a kapcsolatot: infoinfo [at] malyvavirag.humalyvavirag.hu
Titkos és zárt Facebook csoport a terápia témában:
https://www.facebook.com/groups/360804698536521/member-requests
A linkek eléréséhez kattints a címekre!
Érintetteknek a petefészekrákról
Budapesti Nőgyógyászati Daganatsebészeti Központ
SOTE Nőgyógyászati Onkológiai és Daganatsebészeti Osztály
Kívül-belül – Képalkotó eljárások bemutatása
Mit jelent ráktúlélőnek lenni?
Genetikai vizsgálatok a daganatkialakulásra fokozott hajlamot okozó génekkel rendelkező nők számára
Műtét / elsődleges kezelés
Azt, hogy az első terápiás lépés műtét vagy kemoterápia lesz-e, elsősorban a képalkotó vizsgálat eredménye határozza meg, attól függően, hogy milyen kiterjedésű a folyamat, hogyan viszonyul a környező szervekhez, és összességében, hogy daganatmentesség elérhető-e a műtéttel. Amennyiben úgy ítélik meg, hogy ez kivitelezhető, akkor első lépésben műtét történik, mely során a kétoldali petefészkeket, a méhet, a cseplesznek nevezett kötényszerűen lelógó zsíros képződményt, illetve nyirokcsomókat és szükség esetén a hashártya kóros területeit vagy akár bélrészletet is eltávolítanak.
Már leírva is egy nagy beavatkozás ez, mely természetesen igénybe veszi a páciens erejét is, de tapasztalatok alapján pár napos lábadozást követően szépen gyógyulnak, erősödnek a páciensek a műtétből.
Amennyiben a képalkotó alapján daganatmentesség a műtéttel nem érhető el, akkor kemoterápiával kezdődik a kezelés. Ez esetben neoadjuváns kemoterápiának nevezzük a kezelést. Elsősorban ebben az esetben van jelentősége a core-biopsziának, hiszen a szövettani típusnak megfelelő kemoterápiás kezelést kell kezdenünk, mint neoadjuváns kezelés. 3-4 kemoterápiát követően (3 hetente történik kezelés) ismét képalkotó vizsgálatot végeznek, és amennyiben ez alapján a folyamat kiterjedése csökkent, és daganatmentesre operálható a páciens, akkor műtét következik. Ezt intervallum műtétnek nevezzük, amely arra utal, hogy kemoterápiás kezelés ciklusai között történik a beavatkozás, vagyis a műtétet követően a kemoterápiát folytatni kell (további 3 kezeléssel).
HIPEC: ennek angol jelentése: Hyperthermic intraperitoneal chemotherapy. Egyszerre alkalmazzák a kemoterápiás kezelést a műtéttel kombinálva, előrehaladott hasi daganatok kezelésében. Felmelegített rákellenes gyógyszereket infúzióval adnak be, és rövid ideig keringetnek a hasüregben.
A kemoterápiás gyógyszereket körülbelül 42-43 °C-ra melegítik. A rákos sejtek nem képesek kezelni a hőt, ahogy egyébként az egészséges sejtek sem. A hő segít abban is, hogy a gyógyszerek könnyebben belépjenek a sejtjeidbe.
A HIPEC nagy műtét, amely 8-10 óráig vagy még hosszabban tart, altatásban végzik. Először a sebész eltávolít minden látható daganatot. Ezt a lépést nevezzük citoreduktív műtétnek vagy “CRS”-nek. Ezután a hasban felmelegített kemoterápiás gyógyszereket keringetnek.
Orvosod a te egyedi körülményeid alapján dönt a gyógyszerek pontos kombinációjáról, és a testben maradás időtartamáról. A legtöbb esetben a HIPEC 30-120 percig tart. Az egészségügyi csapat ide-oda ringat, hogy megbizonyosodjon arról, hogy a gyógyszerek minden zugba eljutnak. Annak érdekében, hogy a test belső hőmérséklete ez idő alatt alacsony maradjon, egy speciális hűtőtakaróra tesznek.
Ha elegendő idő telik el, a gyógyszerek kiürülnek a hasadból, megtörténik annak összevarrása, majd az intenzív osztályon maradsz egy ideig megfigyelésen. A HIPEC nem jelent minden petefészekdaganatos beteg számára megoldást, a módszer szükségességét szuperspecializált szakemberek csoportjának véleménye alapján érdemes eldönteni.
AZ ALTATÁS
Mi is az az anesztézia?
A szó jelentése érzésnélküliség, vagyis arra szolgál, hogy a fájdalmas vizsgálat vagy műtéti beavatkozás alatt kikapcsolja azokat a jelzéseket, amik a fájdalom érzetét juttatják el az agyunkba.
Az anesztézia lehet általános = altatás, ilyenkor alszol, és semmit nem érzel, érzékelsz a külvilágból, vagy regionális = ilyenkor a testnek egy részét kapcsolják ki az érzések közvetítéséből, ilyen a spinális, epidurális, regionális és a helyi érzéstelenítés.
Mit csinál az aneszteziológus?
- veled egyetértésben megtervezi a műtéthez szükséges érzéstelenítést,
- ellenőrzi az életfunkciókat a műtét/altatás alatt,
- adagolja a gyógyszereket, altatógázokat, szükség esetén antibiotikumokat vagy vérkészítményeket,
- megtervezi a műtét utáni fájdalomcsillapítást,
- felügyeli a műtét utáni állapotodat az őrzőben vagy az intenzív osztályon.
Mi a teendő műtét/ altatás előtt?
- ha dohányzol, minél hamarabb hagyd abba, legjobb hetekkel a tervezett műtét előtt,
- a túlsúly fokozott műtéti rizikót jelent, ha lehet egy könnyű diétával hozd formába magad,
- ha van mozgó vagy törött fogad, keresd fel a fogorvosodat,
- ha van krónikus alapbetegséged, menj el a gondozó orvosodhoz, hogy a lehető legjobb állapotba kerülj a műtét időpontjára.
Mi az az aneszteziológiai ambulancia?
A műtét előtt találkozni fogsz egy aneszteziológussal, aki előzetes felmérést fog végezni az állapotodról, és megbeszélhetsz vele minden részletet az altatással kapcsolatban. Az aneszteziológiai ambulancián a háziorvosi vizsgálathoz hasonló vizsgálat történik, kikérdeznek, megmérik a vérnyomásodat, megnézik a leleteidet. Szinte minden esetben szükséges egy EKG és egy laborvizsgálat műtét előtt, de lehet, hogy egyéb eredményekre is szükség lesz, pl. mellkasröntgen, esetleg szívultrahang, ezt az aneszteziológus dönti el.
Mi történik a műtét előtt, alatt, után?
A műtét előtt már az előző napon valószínűleg be kell feküdnöd a kórházba. Sok helyen már vacsorázni sem lehet a műtét előtti napon, sőt lehet, hogy beöntést vagy hashajtót fogsz kapni. Erre azért van szükség, hogy kiürüljenek a belek, jobb műtéti körülményeket teremtve. Figyelj a folyadékbevitelre, inni a műtét előtt maximum 2 órával még lehet, vizet, teát vagy szűrt gyümölcslevet, igyál eleget!
Már este is, de a műtét reggelén biztosan fogsz kapni egy „bátorító tablettát”, ez segít, hogy könnyebben átvészeld a műtét előtti várakozást.
És amikor eljön az idő, jön érted a műtősfiú! Le kell majd vetkőznöd teljesen, lehet, hogy kapsz egy kórházi hálóinget, de az is lehet, hogy csak jól betakarnak. A műtőben kapsz egy sapkát, ellenőrzik a személyazonosságodat, a csuklódon lévő kis névjegykártyát, egyeztetik a műtét típusát.
Aztán előkészítenek az altatáshoz: EKG-tappancsokat raknak a mellkasodra, vénát biztosítanak, vérnyomásmérőt helyeznek a felkarodra, ami 5 percenként mérni fog, az ujjad hegyére pedig kapsz egy kis csipeszt, ami a vér oxigénszintjét fogja mérni.
Ha epidurális kanült beszéltetek meg, azt ebben a fázisban teszik be. Fel kell majd ülnöd, kapsz egy kis helyi érzéstelenítőt a szúrás helyére, és két csigolya között bevezetik ezt a kis csövecskét, amin keresztül műtét után kaphatsz majd fájdalomcsillapítót.
Ezután jön az altatás: kapsz majd fájdalomcsillapítót, altatószert, és, ha már mélyen elaludtál, izomlazítót is, hogy a lélegeztetőcsövet be tudják helyezni a légcsövedbe. A műtét alatt az aneszteziológus minden életfontos paramétert folyamatosan ellenőrizni fog, ha szükséges, ad még gyógyszert, irányítja a lélegeztetést, folyadékot pótol, mindent megtesz azért, hogy a lehető legjobban bírd a műtétet.
Amikor a sebész befejezte, leállítják a gyógyszerek és altatógázok adagolását, és hagyják, hogy magadtól felébredj. Ébredés után még kába leszel, nem fogsz emlékezni rá, de átkerülsz majd az őrzőbe, ahol még rendszeresen mérik az életfontos paramétereket, lesz rajtad egy oxigénmaszk, és egy szakképzett nővér felügyeli a fájdalomcsillapítást. A hasadból valószínűleg drének lógnak majd ki, kötés lesz rajta, és szinte biztos, hogy hólyagkatétered lesz. Nyugi, semmit nem viszel haza, ezeket mind szépen, fokozatosan eltávolítják majd, de most segítenek.
Az osztályra vissza:
Mikor már minden értéked stabil, és a fájdalom is jól kontrollálható, visszakerülsz a „sima” osztályra. A műtét típusától függ, hogy mikor, de lassan elkezdhetsz kortyolni folyadékot, később ehetsz is pár falatot, szigorúan az előírt diétás szabályok szerint. Ne felejtsd, az egész hasadat megbolygatták, idő kell a beleknek, hogy magukhoz térjenek. Jön majd gyógytornász, lehet, hogy pszichológus, és persze a kezelőorvosod is elmondja majd a műtét menetét.
Lehet az altatásnak szövődménye?
Lehet. Minden orvosi beavatkozásnak lehetnek mellékhatásai és szövődményei, még akkor is, ha mindent elkövetnek, hogy ne legyen. A leggyakoribb mellékhatások: rossz közérzet, szédülés, hányinger, aluszékonyság, fejfájás, ezek rövid idő alatt maguktól is megszűnnek.
Az altatás leggyakoribb szövődménye a torokfájdalom (a lélegeztetőcső miatt) illetve fogsérülés (ez pedig a lélegeztetőcső behelyezésekor alakulhat ki). Ritkán előfordulhat vérnyomásingadozás, szívritmuszavar, szívelégtelenség, allergiás reakció gyógyszerekre, műtét utáni légzési nehézség, ezekre az altatóorvos előre figyelmeztetni fog, ha a műtét jellege vagy az alapbetegségeid miatt fokozott kockázatnak vagy kitéve.
FONTOS:
A nőgyógyászati daganatok kezelése onkológiai centrumban történjen, erre a területre specializálódott nőgyógyász onkológus, klinikai onkológus, daganatsebész által!
Mályvavirág Szakmai Bizottság
A Mályvavirág Alapítvány szorosan együttműködik egészségügyi szakemberekkel - legyen szó akár egy kiadvány elkészítéséről, diagnózis felállításáról, vagy műtétekről, terápiákról, másodvéleményről, intézményi együttműködésről, felvilágosító munkáról, információ szerzésről vagy átadásról.
Keresd bizalommal őket!
https://malyvavirag.hu/szakmai-bizottsag
Onkológiai Centrumok, melyekkel a Mályvavirág Alapítvány együtt dolgozik:
Budapest
Debrecen
Mályvavirágok Közössége a Facebookon - titkos és zárt csoport:
Nőgyógyászati daganattal érintettek csoportja. A tagok beszélgetnek, információkat osztanak meg, kérdeznek, tanácsolnak, segítik egymást. A csoportban szakemberek is jelen vannak, moderált, szabályzattal ellátott közösség a Facebookon.
Itt mindenről szó van, jó és rossz dolgokról is. Lehet aktívan részt venni benne és hátulról figyelni. Ki lehet menni bármikor és újra kérni a felvételt.
Titkos és zárt, nem látszik az adatlapon, ha csatlakozol, és megtalálni sem lehet.
Csoportba bejutás:
1. lépés, hogy like-old a Mályvavirág nyílt oldalt, ha még nem tetted meg,- csak így tudunk a zárt csoportba tenni.
2. lépés: kérjük töltsd ki ezt a kérdőívet: https://forms.gle/uvf6tasEVrpf7j4K6
3. lépés: Facebook értesítés érkezik neked, hogy bejöhetsz a csoportba.
Amennyiben elakadnál, kérjük, vedd fel velünk a kapcsolatot: infoinfo [at] malyvavirag.humalyvavirag.hu
Titkos és zárt Facebook csoport a terápia témában:
https://www.facebook.com/groups/360804698536521/member-requests
Tóth Icó: Libellus - Minden anyuka meggyógyul! - igényelhető a Mályvavirág Alapítványtól
Kemoterápia / elsődleges kezelés
Kemoterápiás szereknek nevezzük azokat a gyógyszereket, melyek hatásmechanizmusuk során károsítják a szervezet osztódó sejtjeit. Ezek a gyógyszerek ugyan minden sejtünkre hatnak, azonban lényegesen kisebb fokban károsítják a normál sejteket, mint a daganatosokat, amelyekkel szemben harcolnak. A kezelés során elpusztul az összes éppen osztódó sejt, azonban a kezelés utáni időszakban az egészséges sejtek az eredeti, normális mennyiségre szaporodnak, míg a daganatsejtekből kevesebb lesz, és számuk lassabban emelkedik a kiindulási értékhez képest.
A kezelés célja a daganatos beteg teljes gyógyulása, a daganatmentes időszak elérése, vagy ennek elmaradása esetén a daganat növekedésének lassítása, leállítása. Meg kell jegyeznünk azt is, hogy olykor csak a tünetek enyhítésére van lehetőségünk.
Kemoterápia csak a daganat szövettani típusának tisztázását követően, bizottsági döntésnek megfelelően adható, hiszen minden kezelést szerv- és szövetspecifikusan választanak ki az orvosok. A kezelési tervet az onkológus csapat állítja fel, ez mindig az adott esettől és a kezelések hatékonyságától függ. A kemoterápiát minden alkalommal a páciensre dozírozzák (adagolják) testfelszín vagy speciális logaritmus alapján.
A kemoterápiának bizony vannak mellékhatásai. Mint minden gyógyszerkészítményre, a kemoterápiára is lehet allergiás a páciens. Sajnos a tenyérviszketéstől, a kipirosodástól a nehézlégzésen, a szívdobogásérzésen, a deréktáji fájdalmon át, a súlyos anafilaxiás reakciókig bármi előfordulhat, azonban szakképzett személyzet áll rendelkezésre, akik ezeket a reakciókat azonnal kezelni tudják.
Amennyiben a beteg rosszul tolerálja a kezelést, a panasz súlyosságától függően akár a kemoterápiás készítmény változtatására is sor kerülhet. A panaszok enyhítésére, kivédésére a kezelés előtt előkészítő gyógyszereket alkalmaznak, amelyek gondoskodnak a gyomor védeleméről, illetve allergia elleni antihisztamint, szteroidot és hányáscsillapító gyógyszert is kap a beteg. Számítani kell arra is, hogy a páciens otthonában további mellékhatások várhatóak. A hányinger, a hányás, a hasmenés és a székrekedés gyakori panasz. Vannak készítmények, melyek alkalmazása a bőr, a haj és a köröm állapotát is érinti, mint a haj elvesztése, vagy a körmök elszíneződése, gombásodása. Nyálkahártya gyulladás, szájszárazság is jelentkezhet. A vérsejteket érintő mellékhatások fokozódnak a felvett kemoterápiák számával, így csökkent fehérvérsejt, vörösvérsejt és vérlemezke számot mutatnak a laborvizsgálatok eredményei. A kemoterápia és a daganat maga is fokozza a trombózis ( vérrögképződés) készséget, így az orvosok vérhígító készítményt alkalmaznak ennek megelőzésére.
Szívizomkárosodás a kardiotoxikus készítmények esetében várható, így szívultrahang-vizsgálattal figyelemmel kísérjük a szív pumpafunkcióját, hiszen csak adott határérték felett adhatóak ezek a készítmények. Vannak olyan gyógyszerek, melyek a perifériás idegeket bántják, így a talp- és az ujjbegyek zsibbadását okozzák. Máj- és vesefunkciós eltérések abból adódhatnak, hogy a kemoterápiás hatóanyagok vagy a májon vagy a vesén keresztül választódnak ki.
A kemoterápia menete
Minden kezeléssorozat egy megbeszéléssel indul, ahol az orvos és a beteg meghatározzák a célt, és megtervezik a kezeléseket. Megbeszélik, hogy milyen mellékhatások várhatók, és minden felmerülő kérdésre választ adnak. Szó esik arról is, hogy a megfelelő táplálkozással hogyan védhetünk ki bizonyos panaszokat, és mivel segíthető még a gyógyulás. Ilyenkor felírják az előkészítő gyógyszereket is, és megbeszélik az adagolásukat. A kezelésekre reggel kell érkezni, mert a gyógyszer vénás infúziós beadása órákat vehet igénybe, de a jó hír, hogy még aznap haza is mehetnek a betegek. Az első kezeléskor beleegyező nyilatkozatot kell a páciensnek aláírnia, esetenként a szívultrahang eredmény is szükséges. Minden kezelés előtt friss laborvizsgálatot végeznek, mely tartalmazza a vérképet, máj- és vesefunkciós paramétereket, ionokat, vizeletvizsgálatot. Amennyiben ezek megfelelőek a kezeléshez, súlymérést követően kiszámolják a kemoterápia dózisát. A betegnek ilyenkor lehetősége van arra, hogy megbeszélje a panaszait orvosával, és megoldást keressenek rá. Ezek után a kezelési lappal a kemoterápiás kezelőbe irányítják a beteget, ahol a gyógyszertárból megrendelt gyógyszer megérkezését követően a nővér beköti az előírt készítményt, amennyiben a beteg vitális paraméterei rendben vannak. A kezelő helyiségek jól felszereltek a beteg ellátására és kényelméhez igazodva.
Amennyiben zavartalanul lefolyt a kezelés, a beteg kézhez kapja az ambuláns lapját, a beutalót, a receptjeit, és otthonába távozhat. Kezelést követően 1 héttel vérkép laborvizsgálat szükséges, annak ellenőrzésére, hogy a kemoterápia milyen mértékben károsította a csontvelőt, és amennyiben szükséges, lehetőség van a csontvelő támogatására.
Kóros értékek: fehérvérsejtszám 2,0 G/l alatt; abszolút neutrofil szám 1,5 G/l alatt; hemoglobin 9,0 g/dl alatt; vérlemezke 100 G/l alatt. A mellékhatások a kezelést követő másnap, harmadnap jelentkeznek változó intenzitással. A páciensek a megbeszélteknek megfelelően járnak el a mellékhatások megjelenésekor, de olykor előfordul, hogy orvosi segítségre van szükségük ezek megoldására, ilyenkor az egészségügyi személyzet a betegek rendelkezésére áll a megadott elérhetőségeken.
A kezelések hatékonyságát képalkotó vizsgálattal, bizonyos tumorok esetén tumormarkerrel követik. Amennyiben rezisztencia alakul ki egy készítménnyel szemben, vagyis a tumor nem reagál megfelelően a kezelésre, terápiaváltásra kényszerülnek, ezzel kapcsolatban az orvos kimerítő tájékoztatást fog adni betegének.
Kemoterápiás kezelésfajták
Neoadjuváns kemoterápia: a rosszindulatú daganat felismerését követően kemoterápiát választunk első kezelési módnak, ha a műtét azonnal nem kivitelezhető. A kemoterápia hatását képalkotó vizsgálatokkal ellenőrizzük, és az eredmények alapján döntünk a műtétről, melyet további kemoterápia követ.
Adjuváns kemoterápia: a daganatos betegségben a műtétet követő kezelés, amikor az operációt követően kezelést javasolunk, hogy a kiújulás esélyét csökkentsük. Mindig fix alkalom, a kezelés elején tudjuk, mikor lesz vége.
Elsővonalbeli kemoterápia: a daganat felfedezésekor, vagy műtétet követően visszamaradt daganat esetén az elsőként választandó, leggyakrabban használt kemoterápiás szerekre vonatkozik. Ha rezisztencia alakul ki a gyógyszer ellen, akkor hatóanyagot kell váltanunk.
Többedvonalbeli kezelés: rezisztencia miatt gyógyszerváltást követően adott gyógyszer, mely tumormentességig vagy rezisztenciáig, a daganatos betegség rosszabbodásáig adható.
PARÓKA/KENDŐ:
Paróka:
A parókát/kendőt bizonyos kezelések mellé felírják receptre, így kedvezményesebb áron lehet hozzájutni. A receptet már az első kezelés alkalmával megkapják a betegek, és maguk választanak üzletet és parókát. A kedvezmény mértéke üzletenként eltérő lehet. Érdemes az első kezelést követően parókákat próbálni, mert általában az első kezelést követő 10-14. napon szinte a teljes hajkoronát elveszti a páciens. A parókát értékesítő üzletekben nagyon tapintatosak és segítőkészek az alkalmazottak. Érdemes több fazont is próbálni, hogy kialakuljon, melyik a legkomfortosabb viselet számunkra. Azzal is számolni kell, hogy a paróka próbálásakor még megvan a hajunk, viszont amikor már viseljük magát a parókát, nem lesz olyan hajtömeg alatta. A paróka alá - hogy ne irritálja a fejbőrt - lehet nylon harisnya anyagból készült kis sapkát venni.
Van igazi hajból készült és műhajból készült paróka. A műhajból készült paróka ápolása nagy odafigyelést igényel: extrém hőhatásnak nem szabad kitenni, hajszárítóval és hajvasalóval általában nem formálható, azonban speciális készítményekkel mosható. A paróka fazonját megtartja mindenféle formázás nélkül is a mosást követően. A valódi hajból készült paróka ápolása nagyon hasonlít a saját hajunk ápolásához.
Kendő:
A paróka mellett/helyett lehetőség van kendő viselésére is. Ebből is többféle megoldás létezik. Vannak előre gyártott kendők, amiket csak, mint egy “sapka” kell felvenni, és esetleg hátul a tarkónál megkötni. Általában puha pamut anyagból, esetleg öko-pamutból készülnek, hogy a kopasz fejbőrön kényelmes viseletet adjanak. Nagyon komfortos viselet, akár többféle szín és fazon is beszerezhető, így változatosabbá tehető az öltözködésünk. Az előre megvarrt kendők mellett nagyon praktikus a normál női kendők/sálak viselése is. Ezek általában téglalap alakú, hosszú kendők, amikkel megfelelő kötési technikával olyan végeredményt érhetünk el, mint egy előre megvarrt kendővel. Ezek lehetnek pamutból vagy selyemből, esetleg keverék anyagból készült vékony sálak is. Nagyon komfortos a viselésük.
Turbán:
A kendők mellett lehet a parókaárusító üzletekben ún. turbánokat is vásárolni. Ezek általában - évszaknak megfelelően - vastagabb vagy vékonyabb pamutból készült kis “sapkák”, némi rafinériával megvarrva. Nagyon egyszerű a viselésük, mert tényleg, csak, mint egy sapkát kell felvennünk.
Mi szól mellette és ellene?
Paróka
Mellette:
- egy jól megválasztott fazon esetében kívülálló számára szinte észrevehetetlen, úgy tudjuk viselni, mint a saját hajunkat
- nem igényel napi fazon beállítást
- könnyű kezelés
- bizonyos munkakörökben, vagy, ha nem szeretnénk a környezetünk tudomására juttatni betegségünket egy optimális megoldás
- szinte mindenféle tevékenység végezhető vele, akár sportolás is
- recepttel támogatott a vásárlása
Ellene:
- melegebb viselet
- nehéz az eredeti hajszínünkhöz és formánkhoz nagyon hasonlót találni
- speciális eszközöket igényel az ápolása
- megosztóbb a viselése
- nem mindenki tudja elviselni a fejbőrén a parókát
- “idegen érzés” a tükörbe nézve
Kendő
Mellette:
- nagyon komfortos viselet
- többféle kendővel változatosabbá tehetjük az öltözködésünket
- nem meleg a nyári napokban sem
- olcsóbban beszerezhető
- a kezelések befejeztével is tovább hordható sálként/női kendőként, mint a sziluettünk része
- szépen kiemeli az arc vonásait
- mindenféle tevékenység végezhető benne
- nem igényel kifejezett ápolást, mosható, gyorsan szárad
- könnyen variálható
Ellene:
- egyértelműsíti a betegségünket
- támogatás nem kérhető rá
- picivel több időt igényel a felkötése (kivéve, ha előre varrt kendőről van szó)
- a fület eltakarja, ami zavaró lehet
Fontos:
Védeni kell a napsugárzástól a bőrt, mert a citosztatikumok fényérzékenyek, és hamarabb bomlanak le fény hatására a szervezetünkben.
FONTOS:
A nőgyógyászati daganatok kezelése onkológiai centrumban történjen, erre a területre specializálódott nőgyógyász onkológus, klinikai onkológus, daganatsebész által!
Mályvavirág Szakmai Bizottság
A Mályvavirág Alapítvány szorosan együttműködik egészségügyi szakemberekkel - legyen szó akár egy kiadvány elkészítéséről, diagnózis felállításáról, vagy műtétekről, terápiákról, másodvéleményről, intézményi együttműködésről, felvilágosító munkáról, információ szerzésről vagy átadásról.
Keresd bizalommal őket!
https://malyvavirag.hu/szakmai-bizottsag
Onkológiai Centrumok, melyekkel a Mályvavirág Alapítvány együtt dolgozik:
Budapest
-
Országos Onkológiai Központ: https://onkol.hu/
-
SOTE/Semmelweis Egyetem Radiológiai és Onkoterápiás Klinika: https://semmelweis.hu/klinikaikozpont/
-
Uzsoki Utcai Kórház: http://www.uzsoki.hu/onkologiai-gondozo
-
Dél Pesti Centrumkórház, Egyesített Szent László és Szent István Kórház
Debrecen
-
Debreceni Egyetem Klinikai Központ Szülészeti és Nőgyógyászati Klinika: https://noiklinika.unideb.hu/
Mályvavirágok Közössége a Facebookon - titkos és zárt csoport:
Nőgyógyászati daganattal érintettek csoportja. A tagok beszélgetnek, információkat osztanak meg, kérdeznek, tanácsolnak, segítik egymást. A csoportban szakemberek is jelen vannak, moderált, szabályzattal ellátott közösség a Facebookon.
Itt mindenről szó van, jó és rossz dolgokról is. Lehet aktívan részt venni benne és hátulról figyelni. Ki lehet menni bármikor és újra kérni a felvételt.
Titkos és zárt, nem látszik az adatlapon, ha csatlakozol, és megtalálni sem lehet.
Csoportba bejutás:
1. lépés, hogy like-old a Mályvavirág nyílt oldalt, ha még nem tetted meg,- csak így tudunk a zárt csoportba tenni.
2. lépés: kérjük töltsd ki ezt a kérdőívet: https://forms.gle/uvf6tasEVrpf7j4K6
3. lépés: Facebook értesítés érkezik neked, hogy bejöhetsz a csoportba.
Amennyiben elakadnál, kérjük, vedd fel velünk a kapcsolatot: infoinfo [at] malyvavirag.humalyvavirag.hu
Titkos és zárt Facebook csoport a terápia témában:
https://www.facebook.com/groups/360804698536521/member-requests
Fenntartó terápia / elsővonalbeli kezelés
Olyan daganatellenes kezelés, amelynek célja, hogy folyamatos alkalmazásával megakadályozza a primer daganat kiújulását, vagy lelassítsa a daganat növekedését. A fenntartó kezelést a betegség progressziójáig, vagy elfogadhatatlan mértékű mellékhatások megjelenéséig alkalmazzuk. A nőgyógyászati daganatok esetében több fajta fenntartó kezelés is létezik, ilyen pl. az érképződést gátló, a PARP-gátló kezelések vagy az immunterápia. A fenntartó kezelések nem minden nőgyógyászati daganatos betegségben érhetőek el, s adott betegségen belül is vannak olyan előre meghatározott betegcsoportok, akik számára ez a kezelés előnyt jelenthet, mint pl. a BRCA-mutációt hordozó, bizonyos szövettani típussal rendelkező petefészekrákos nők esetében a PARP-gátlók alkalmazása. Kiszerelési formájukat tekintve is különbözőek lehetnek, van amelyiket infúzióban adják be, de van olyan is, amelyiket szájon át alkalmaznak (kapszula/tabletta formájában). Ezen kezelések alkalmazása szigorú feltételekhez és gyakori ellenőrzésekhez kötött. Az onkoteam ítéli meg, hogy kinél alkalmazhatóak ezek a kezelések, és a beteg a kezelő orvossal közösen nyújtja be az engedélyeket az illetékes hatóságnak/hatóságoknak (NEAK, OGYÉI).
A fenntartó terápiák lehetnek elsővonalbeliek, amikor első kezelésként adják és lehetnek másodvonalbeliek, amikor kiújuláskor adják.
I. Érújraképződés-gátló
VEGF-gátló
A rákos sejt a működéséhez szükséges tápanyagokat kezdetben a környezetéből veszi fel. A tumor növekedése során a tumort alkotó rákos sejtek egy idő után már nem lesznek képesek elegendő tápanyagot felvenni a környezetükből. Ekkor olyan jeleket kezdenek kibocsátani magukból, amik arra késztetik a szervezetet, hogy ereket növesszen a tumor köré, és ezeken keresztül táplálja azt. Az egyik ilyen anyag, amit jelként bocsát ki a tumor, a VEGF (vaszkuláris endotheliális növekedési faktor). A VEGF az egészséges szervezetben is jelen van, ez segít szabályozni az erek növekedését fejlődésünk során. A daganat esetében kórosan sok VEGF szabadul fel, és a tumor körül szabálytalan, kusza érhálózat alakul ki. Ez felborítja a tumorsejtek körüli ozmotikus nyomásviszonyokat is. Emiatt a gyógyszermolekulák is nehezebben tudnak kilépni a tumor körüli erekből, és kifejteni hatásukat a rákos sejtekre.
Vannak olyan biológiai terápiák, melyeknek célja, hogy a szervezetben keringő VEGF-molekulákat megkössék. Ezzel megszüntetik a jelet, amit a tumor bocsát ki magából. Ennek hatására a tumort behálózó erek növekedése megszűnik, a már kialakult erek visszafejlődnek, rendezetté válnak, így a tumor tápanyagellátása megszűnik, a tumorsejtek nem osztódnak tovább, tápanyag híján elpusztulnak, helyreáll a tumor körüli ozmotikus nyomás is. Ezek után már más rák elleni gyógyszerek is könnyebben elérik a rákos sejteket, és hatékonyabban tudják kifejteni a hatásukat a tumorra.
A VEGF-gátlók biológiai terápiák, fehérje természetű gyógyszerek. Használatukhoz nincs szükség genetikai vizsgálatokra. BRCA-mutációtól függetlenül alkalmazhatóak, többféle daganattípusban használhatóak, például vastagbéldaganat, nem kissejtes tüdődaganat, emlődaganat, hám eredetű petefészekdaganat, méhnyakrák.
Hatékonyabb a terápia, ha biztosítjuk az érújdonképződés gátlását (azaz gátoljuk a tumor körüli erek növekedését), és eközben más tumor elleni terápiával (kemoterápia, célzott terápiák) igyekszünk megakadályozni a tumorsejtek osztódását, illetve elpusztítjuk azokat. Ezért általában ezeket a terápiákat a nagyobb siker érdekében kombinálva használják.
Ezek a gyógyszerek Magyarországon is elérhetőek, sajnos nem a legolcsóbb terápiák közé tartoznak jelenleg. A finanszírozásukat a NEAK egyedi méltányosság keretein belül biztosítja, az egyedi méltányosságra vonatkozó kérelmet az onkológus indíthatja el, az onkoteam javaslata alapján. A kérelem benyújtása után 60 nap áll rendelkezésére az elbírálására. Pozitív válasz esetén kezdődhet el a terápia.
A VEGF-gátló gyógyszer egy oldat, amit infúzióban hígítva adnak be intravénásan, két- vagy 3 háromhetente az onkológiai kúraszerű ellátás keretében. Az infúzió önmagában vagy más kemoterápiás szerekkel együtt adva is alkalmazható, a kezelés időtartamát protokollok szabályozzák.
A VEGF-gátló gyógyszernek lehetnek mellékhatásai, okozhat magas vérnyomást, elősegítheti sipolyok kialakulását a bélrendszerben, vagy a hüvely és a bél között, megváltoztathatja a véralvadási rendszer működését, így vérrögképződésre hajlamosíthat. Ennek alapján az onkológus nem minden esetben javasolja a használatát, a kockázatok mérlegelése itt is fontos. A kezelőorvosodat minden furcsa tünetről tájékoztatnod kell, bármilyen onkológiai kezelésben is van részed!
Az engedélyezési „csomagot” az onkológusod állítja össze, és Neked is alá kell írni. Az engedélyt 3 majd 6 hónapos ciklusokra adják meg. A gyógyszerár-támogatási kérelmen mindig szerepeljen a telefonszámod és az e-mail címed. A kérelemről a NEAK ügyfélszolgálat telefonon ad tájékoztatást (kedd és csütörtök 9-15 óra között, a 06-1-298-2438-as telefonszámon).
Méltányossági kérelem beadásának menete:
Amikor a kivizsgálás során a rosszindulatú daganat diagnózisát megkapja a beteg (szövettani eredmény alapján általában), akkor a kezelés menetéről onkoteam kell, hogy döntsön (onkológus, sebész/nőgyógyász, patológus, radiológus, sugárterápiás szakember van benne). Itt dől el, hogy operálható vagy sem, kell-e a tervezett műtét előtt kemoterápiát kapni, vagy sem, milyen kemoterápia legyen, terveznek-e fenntartó kezelést. Ha van műtét előtti kemoterápia, akkor is kapsz még a műtét után is (általában 3 előtte, 3 utána, de ez is mindig egyénre szabott onkoteam-döntés).
Gyógyszer-finanszírozás formái Magyarországon:
- Járóbeteg gyógyszerellátás
- Egyedi méltányosság
- Fekvőbeteg intézmény
- HBCS finanszírozása
- Extrafinanszírozása
- Különkeretes gyógyszerek (hepatitis, vérzékenység)
- Tételes gyógyszerek (a NEAK természetben biztosítja)
Egyedi méltányosság kérhető
Magyarországon forgalomba hozatali engedéllyel rendelkező, de nem támogatott, különleges táplálkozási igényt kielégítő tápszerek, gyógyszerek árához
Magyarországon forgalomba hozatali engedéllyel NEM rendelkező, de az OGYÉI véleménye/engedélye alapján rendelhető készítmények árához (egyedi import)
Indikáción túl (off-label) rendelt gyógyszerek árához
A MEGÁLLAPÍTOTT TÁMOGATÁS ÖSSZEGÉVEL KEVESEBB TÉRÍTÉSI DÍJAT KELL A BETEGNEK FIZETNI, és utólag a támogatás összegét a forgalmazó/gyógyszertár és a NEAK elszámolja.
Egyedi méltányosság – dokumentáció
A kérelmet a kezelőorvos adja be
Célszerű az írásbeli kérelemhez már a benyújtásával egyidejűleg csatolni valamennyi kötelező mellékletet, és megadni a megfelelő adatokat, mert azok nélkül nem lehet a kérelmet elbírálni.
A kérelmet írásban a meghatározott mellékletekkel együtt kell benyújtani a NEAK-nak címezve (Nemzeti Egészségbiztosítási Alapkezelő Ártámogatási Főosztály 1139 Budapest, Váci út 73/A., Postafiók: 1565 Budapest).
A kérelem elektronikus kapcsolattartás keretében (a magyarorszag.hu kormányzati portál ügyfélkapu funkciójának kialakításáig) a meltanyossag [at] neak.gov.hu email címen nyújtható be. A kérelem elektronikus benyújtása esetén is csatolni kell valamennyi szükséges mellékletet.
- Betegkérelem-beteg aláírásával
- a beteg neve, lakcíme és TAJ száma;
- gyógyszer kiadására a beteg által megjelölt gyógyszertár megnevezése (célszerű ilyen támogatású gyógyszerek forgalmazásában gyakorlott patikát választani);
- az igényelt gyógyszerkészítmény neve;
- tartalmazhatja a beteg elérhetőségét (telefonszám, e-mail cím).
- Szakorvosi igénylőlap
- beteg személyes adatai, TAJ száma;
- igényelt gyógyszer neve, hatáserőssége, kiszerelése;
- igényelt gyógyszer dózisa (szükség esetén testsúly ill. testfelület megjelölése);
- támogatás időtartama;
- diagnózis (BNO kód);
- igénylő orvos neve, orvosi pecsétszáma, szakvizsgájának megnevezése, elérhetősége (munkahelyének megnevezése, címe, telefonszáma, esetleg e-mail címe).
- Kórtörténeti összefoglaló
- melyben a szakorvos igazolja, hogy a biztosított kizárólag az igényelt készítménnyel kezelhető hatékonyan (3 hónapnál nem régebbi);
- ismételt méltányossági kérelem esetén az adott terápia hatására bekövetkezett állapotváltozás leírása.
- Leletek másolata
- a diagnózis ill. a kérelem szerinti terápia vagy terápiaváltás szükségessége igazolása céljából (a beteg aktuális státuszának igazolásán túl a támogatás hosszabbítása esetén az összehasonlítást is segíti);
- ismételt méltányossági kérelem esetén csak a megelőző kérelem benyújtása óta eltelt időszakban bekövetkezett állapot-változást dokumentáló leletek másolata szükséges.
- Vény
- a kért támogatási időszakra szóló, de vényenként 30 napi vagy 1 ciklusnyi terápiás mennyiséget tartalmazhat;
- szabályszerűen (BNO!);
- egyedi jogcímen;
- ha indikáción túli, akkor „off label” megjelölés és helyettesíthetőség megtiltása!
Elbírálás:
- A kérelem beérkezését követő naptól számított 60 napon belül.
- Indikáción túli gyógyszerrendelés egyszerűsített eljárási esetében 12 napon belül.
- Életet veszélyeztető sürgős esetben soron kívül, azonban a szükséges dokumentumokat a beteg vagy képviselője utólag köteles csatolni.
- A megállapított méltányossági ártámogatás korlátozott időtartamra, első alkalommal legfeljebb egy évre állapítható meg.
II. PARP-gátlók
A PARP-gátlók célzott molekuláris onkológiai gyógyszerek. Ez azt jelenti, hogy nem általánosan hatnak minden osztódó sejtre, mint a kemoterápiás szerek (hiszen ezek ugyanúgy hatnak a daganatos és a nem daganatos sejtekre is), hanem célzottan a daganatsejtekre.
A PARP jelentése: poli ADP-ribóz polimeráz, de ezzel az elnevezésével nem igen fogsz találkozni.
A PARP-enzimek olyan fehérjék, amelyek segítenek a sejtosztódás során létrejött DNS törések (károsodások) kijavításában. A PARP-gátlókat olyan daganatok kezelésében vezették be először, ahol egyébként is már genetikailag létezett egy hiba a javítómechanizmusban (BRCA-mutációk).
Ha hiba van a javítómechanizmusban, akkor az a jó, ha a sejt elhal. De a sejt nem tud elhalni, ha mégis “javítgatják”.
A BRCA1 és BRCA2 gének hasonló funkciójú javítófehérjéket kódolnak, mint a PARP, és azok az emberek, akiknél BRCA-mutáció áll fenn, hajlamosabbak bizonyos daganatfajták kialakulására, ezek az emlőrák, petefészekrák, petevezető- vagy primer hashártya eredetű rákok (a továbbiakban összesítve petefészekrákokként hivatkozva), prosztatarák, hasnyálmirigyrák. A daganatsejtek, melyekben DNS mutáció van, eleve nehezebben képesek a sejtosztódás során kialakuló hibákat kijavítani, így ha a PARP-enzimeket is blokkolják, a DNS feltöredezik, és a daganatos sejt elpusztul.
A BRCA1 és 2 mutáció lehet veleszületett vagy szerzett, az utóbbi csak a tumorban van jelen.
A veleszületett BRCA-mutáció öröklődhet, ez vérvétellel kimutatható, a vizsgálatot molekuláris genetikai laboratóriumokban végzik, az onkológus javaslatára.
A szerzett mutáció, amely a tumorszövetben alakul ki a későbbiekben, a műtét során vett szövetmintából mutatható ki, ezt onkológiai centrumok patológiai laboratóriumaiban tudják kimutatni.
Mindkét vizsgálat az egészségbiztosítás keretében ingyenes - bár van magánfinanszírozott formában is - és a későbbi kezelés meghatározása miatt jelentős információ. Amennyiben a családban előfordult bármilyen ágon emlő- vagy petefészekrák, aránylag fiatal korban, mindenképpen érdemes elvégeztetni ezt a vizsgálatot, sőt, a gyermekeidre is gondolj, hiszen ők is örökölhetik. Az egyenesági hozzátartozók és a testvérek szűrését is a molekuláris genetikai laboratóriumok NEAK-finanszírozás keretében elvégzik.
Ezen biológiai kezelések szigorú feltételekhez kötöttek (alább részletezzük), és a kezeléshez az engedély egyedi méltányossági kérelem benyújtását követően kapható meg. Ezeket az adminisztratív lépéseket (a mintából végzett tumorgenetikai vizsgálat, az egyedi méltányossági kérelem összeállítása) a kezelőorvos végzi el, az alábbi tájékoztató segítség lehet abban, hogy mely esetekben jön szóba az ilyen irányú kezelés.
Amennyiben úgy érzed, hogy az alábbi kezelések valamelyike szóba jöhet az esetedben, akkor fordulj bizalommal valamelyik, a Mályvavirág Alapítvánnyal kapcsolatban álló petefészekrák centrumhoz. Fontos tudnod, hogy Magyarországon a NEAK-finanszírozott ellátás keretében mindenkinek joga van másodvéleményt kérni, másik szakembert felkeresni. Ha úgy érzed, nem vagy elégedett, nem vagy biztos benne, hogy minden lehetőséget ismertettek Veled, vagy csak egyszerűen nem szimpatikus a kezelőorvosod, segítünk másik szakembert találni. Az orvos-beteg kapcsolat bizalmi kapcsolat, ami nem csak professzionális szinten befolyásolja a gyógyulásodat.
Amennyiben grade 2-3 (magas malignitású, szövettanilag differenciálatlan) hám eredetű petefészekrákod van, a kezelése folyamán több ponton is szóba jön a PARP-gátlókkal történő kezelés.
A törvény szerint minden onkológiai betegséggel kapcsolatos döntés onkológiai bizottsági (ún. onkoteam = onkológus szakorvos, daganatsebész szakorvos, patológus szakorvos) véleményezés után történhet, így ez értelemszerűen vonatkozik a fenntartó kezelésekre is.
1. Ha előrehaladott hám eredetű petefészekrákod van (III. és IV. stádium), örökletes vagy a daganatban kialakult BRCA 1 / 2 mutációval, és a daganat reagál az első műtétet követő elsővonalbeli platinabázisú kemoterápiára, úgy PARP-gátló fenntartó kezelés adható. A PARP-gátló kezelést ilyenkor önmagában adják fenntartó kezelésként.
2. A PARP-gátló kezelés kombinálható az érképződést gátló, ún. VEGF-gátlószerekkel is. Ez akkor jön szóba, ha a hám eredetű petefészekrák miatt végzett első műtétnél nem sikerült teljes tumormentességet elérni, örökletes vagy a daganatban kialakult BRCA 1 / 2 mutáció, vagy egyéb homológ javítórendszerben mutáció igazolható, és a daganat reagál az első vonalban adott VEGF-gátlóval kombinált platinabázisú kezelésre.
3. Bizonyos esetekben BRCA 1 / 2 mutáció hiányában is szóba jön a PARP-gátlóval végzett fenntartó kezelés, azonban ezekben az esetekben a hatásosság elmarad a BRCA-mutáció esetében tapasztalttól.
Amennyiben szóba jönnek a PARP-gátlókkal végzett fenntartó kezelések, úgy a kemoterápiás kezelés (rendszerint 6 ciklus) legkésőbb 4. ciklusáig a kivett daganatból tumorgenetikai vizsgálatot kell kérjen a kezelőorvos, mert a vizsgálat és az engedélyezés időigényes folyamata miatt így biztosítható, hogy a kemoterápiás kezelés után a szükséges 8 héten belül megkapd a kezelést, és ne csússz ki az időablakból.
Az engedélyezési „csomagot” az onkológusod állítja össze, és Neked is alá kell írni. Az engedélyt 3, majd 6 hónapos ciklusokra adják meg. A gyógyszerár-támogatási kérelmen mindig szerepeljen a telefonszámod és az e-mail címed. A kérelemről a NEAK ügyfélszolgálat telefonon ad tájékoztatást (kedd és csütörtök 9-15 óra között, a 06-1-298-2438-as telefonszámon).
A PARP-gátlókkal végzett kezelés elindításának is vannak ellenjavallatai, erről kezelőorvosod tájékoztat, pl. ha a megelőző kemoterápiás kezelési sorozat nehezen uralható csontvelő-elégtelenséget okozott.
A PARP-gátlókkal végzett fenntartó kezelések általában jól tolerálhatóak, a leggyakoribb előforduló mellékhatások a csontvelő visszafogott működésére vezethetők vissza (elsősorban vérszegénység, illetve a fehérvérsejtszám csökkenése), mely fertőzésekre hajlamosíthat, illetve a betegek egy részénél emésztési panaszok, hányinger, hasmenés, fáradtság, étvágytalanság jelentkezhetnek. Mellékhatások észlelése esetén konzultálj a kezelőorvossal a teendőkről!
Fontos kényelmi szempont, hogy a kezelés szájon át történik, és nem szükséges infúziós kezelésekre a kórházba járni. A kezelés alatt rendszeres vérképvizsgálatot fognak végezni (az első évben havonta) a mellékhatások észlelésére. Szükség esetén a kezelőorvos az előírt gyógyszer mennyiségének csökkentését írhatja elő. A kezelés folyamatosan adható, amíg a tumort gátolja, ennek igazolására állapotodat háromhavonta CT vizsgálatokkal ellenőrzik. Azon betegek esetében, ahol a kezdeti CA125 tumormarker érték emelkedett volt, ennek ellenőrzését is felhasználják az utánkövetésben.
A PARP-gátlókkal végzett fenntartó kezelés időtartama általában 2 év, de hosszabb ideig is alkalmazható. Jelenleg is folynak kutatások, klinikai vizsgálatok, amelyekben PARP-gátlókat vizsgálnak önmagukban vagy más gyógyszerekkel együtt adva.
A PARP-gátló kezelések nem csak a betegségmentes túlélés növekedésében hatékonyak, de bizonyítottan és jelentősen növelik a betegek teljes túlélését is.
Méltányossági kérelem beadásának menete:
Konkrét esetben újonnan diagnosztizált petefészekrák esetén ez úgy néz ki, hogy amikor a kivizsgálás során a rosszindulatú daganat diagnózisát megkapja a beteg (szövettani eredmény alapján általában), akkor a kezelés menetéről onkoteam kell, hogy döntsön (onkológus, sebész/nőgyógyász, patológus, radiológus van benne). Itt dől el, hogy operálható vagy sem, kell-e a tervezett műtét előtt kemoterápiát kapni, vagy sem, milyen kemoterápia legyen, terveznek-e fenntartó kezelést. Ha van műtét előtti kemoterápia, akkor is kapsz még a műtét után is (általában 3 előtte, 3 utána, de ez is mindig egyénre szabott onkoteam-döntés). Ideálisan legkésőbb az első onkoteamen döntenek arról is, hogy végezzenek-e BRCA-vizsgálatot, és ezt el is indítják (kb. 1 hónapon belül van eredmény). Az Egyedi Méltányossági Kérelem beadására akkor kerülhet sor, ha pozitív a BRCA-lelet, és a beteg megkapott kb. 4 platinabázisú kezelést (ez attól is függ, hogy hány kezelést terveznek), és a kontroll CT, tumormarker is rendben van. Lehet, hogy míg a kérelmed a NEAK jóváhagyásra vár, még kapsz további kezeléseket. Ha megjön az engedély, leghamarabb az utolsó kezelés után 3 héttel kezdhető el a fenntartó PARP-kezelés, ha a vérképed rendeződött, de erre van egyébként 8 hét (3-8 hét között kell elkezdeni a kezelést).
Gyógyszer-finanszírozás formái Magyarországon:
- Járóbeteg gyógyszerellátás
- Egyedi méltányosság
- Fekvőbeteg intézmény
- HBCS finanszírozása
- Extrafinanszírozása
- Különkeretes gyógyszerek (hepatitis, vérzékenység)
- Tételes gyógyszerek (a NEAK természetben biztosítja)
Egyedi méltányosság kérhető
Magyarországon forgalomba hozatali engedéllyel rendelkező, de nem támogatott, különleges táplálkozási igényt kielégítő tápszerek, gyógyszerek árához
Magyarországon forgalomba hozatali engedéllyel NEM rendelkező, de az OGYÉI véleménye/engedélye alapján rendelhető készítmények árához (egyedi import)
Indikáción túl (off-label) rendelt gyógyszerek árához.
A MEGÁLLAPÍTOTT TÁMOGATÁS ÖSSZEGÉVEL KEVESEBB TÉRÍTÉSI DÍJAT KELL A BETEGNEK FIZETNI, és utólag a támogatás összegét a forgalmazó/gyógyszertár és a NEAK elszámolja.
Egyedi méltányosság – dokumentáció
A kérelmet a kezelőorvos adja be
Célszerű az írásbeli kérelemhez már a benyújtásával egyidejűleg csatolni valamennyi kötelező mellékletet és megadni a megfelelő adatokat, mert azok nélkül nem lehet a kérelmet elbírálni.
A kérelmet írásban a meghatározott mellékletekkel együtt kell benyújtani a NEAK-nak címezve (Nemzeti Egészségbiztosítási Alapkezelő Ártámogatási Főosztály 1139 Budapest, Váci út 73/A., Postafiók: 1565 Budapest).
A kérelem elektronikus kapcsolattartás keretében (a magyarorszag.hu kormányzati portál ügyfélkapu funkciójának kialakításáig) a meltanyossag [at] neak.gov.hu email címen nyújtható be. A kérelem elektronikus benyújtása esetén is csatolni kell valamennyi szükséges mellékletet.
- Betegkérelem-beteg aláírásával
- a beteg neve, lakcíme és TAJ száma;
- gyógyszer kiadására a beteg által megjelölt gyógyszertár megnevezése (célszerű ilyen támogatású gyógyszerek forgalmazásában gyakorlott patikát választani);
- az igényelt gyógyszerkészítmény neve;
- tartalmazhatja a beteg elérhetőségét (telefonszám, e-mail cím).
- Szakorvosi igénylőlap
- beteg személyes adatai, TAJ száma;
- igényelt gyógyszer neve, hatáserőssége, kiszerelése;
- igényelt gyógyszer dózisa (szükség esetén testsúly ill. testfelület megjelölése);
- támogatás időtartama;
- diagnózis (BNO kód);
- igénylő orvos neve, orvosi pecsétszáma, szakvizsgájának megnevezése, elérhetősége (munkahelyének megnevezése, címe, telefonszáma, esetleg e-mail címe).
- Kórtörténeti összefoglaló
- melyben a szakorvos igazolja, hogy a biztosított kizárólag az igényelt készítménnyel kezelhető hatékonyan (3 hónapnál nem régebbi);
- ismételt méltányossági kérelem esetén az adott terápia hatására bekövetkezett állapotváltozás leírása.
- Leletek másolata
- a diagnózis ill. a kérelem szerinti terápia vagy terápiaváltás szükségessége igazolása céljából (a beteg aktuális státuszának igazolásán túl a támogatás hosszabbítása esetén az összehasonlítást is segíti);
- ismételt méltányossági kérelem esetén csak a megelőző kérelem benyújtása óta eltelt időszakban bekövetkezett állapot-változást dokumentáló leletek másolata szükséges.
- Vény
- a kért támogatási időszakra szóló, de vényenként 30 napi vagy 1 ciklusnyi terápiás mennyiséget tartalmazhat;
- szabályszerűen (BNO!);
- egyedi jogcímen;
- ha indikáción túli, akkor „off label” megjelölés és helyettesíthetőség megtiltása!
Elbírálás:
- A kérelem beérkezését követő naptól számított 60 napon belül.
- Indikáción túli gyógyszerrendelés egyszerűsített eljárási esetében 12 napon – belül.
- Életet veszélyeztető sürgős esetben soron kívül, azonban a szükséges dokumentumokat a beteg vagy képviselője utólag köteles csatolni.
- A megállapított méltányossági ártámogatás korlátozott időtartamra, első alkalommal legfeljebb egy évre állapítható meg.
Mályvavirágok Közössége a Facebookon - titkos és zárt csoport:
Nőgyógyászati daganattal érintettek csoportja. A tagok beszélgetnek, információkat osztanak meg, kérdeznek, tanácsolnak, segítik egymást. A csoportban szakemberek is jelen vannak, moderált, szabályzattal ellátott közösség a Facebookon.
Itt mindenről szó van, jó és rossz dolgokról is. Lehet aktívan részt venni benne és hátulról figyelni. Ki lehet menni bármikor és újra kérni a felvételt.
Titkos és zárt, nem látszik az adatlapon, ha csatlakozol, és megtalálni sem lehet.
Csoportba bejutás:
1. lépés, hogy like-old a Mályvavirág nyílt oldalt, ha még nem tetted meg,- csak így tudunk a zárt csoportba tenni.
2. lépés: kérjük töltsd ki ezt a kérdőívet: https://forms.gle/uvf6tasEVrpf7j4K6
3. lépés: Facebook értesítés érkezik neked, hogy bejöhetsz a csoportba.
Amennyiben elakadnál, kérjük, vedd fel velünk a kapcsolatot: infoinfo [at] malyvavirag.humalyvavirag.hu
Titkos és zárt Facebook csoport a terápia témában:
https://www.facebook.com/groups/360804698536521/member-requests
Utánkövetés
A műtéti és gyógyszeres (kemoterápiás) kezelést követően a daganatmentes betegeknél rendszeres kontrollvizsgálatok javasoltak.
Ezek a vizsgálatok azért fontosak, mert így a kezelés okozta késői szövődmények (például kemoterápia-okozta idegkárosodás, késői műtéti összenövések) idejekorán felismerhetőek; életminőséget javító kiegészítő terápiát (pl. pszichoterápia, fájdalomterápia) tudunk javasolni; és a daganat kiújulását idejében fel lehet ismerni.
A legtöbb szakértő és daganatellátással foglalkozó nemzetközi szervezet ajánlása alapján az utógondozás során a következők elvégzése mindenképpen javasolt:
- Panaszok részletes kikérdezése
- Nőgyógyászati szakvizsgálat során a kismedencei szervek elhelyezkedését, valamint a hashártya érintettséget lehet közelítőleg felmérni. Tükörvizsgálattal a hüvelycsonk vizsgálható.
Ritkán egyidejűleg végzett hüvelyi és végbél-vizsgálatra is szükség van.
A kezelés befejezése utáni első két évben háromhavonta, a következő három évben hathavonta, majd öt év elteltével évente szükséges ezen vizsgálatok elvégzése.
- Az általános ajánlások szerint panaszmentes betegnél további képalkotó vizsgálatokra nincs szükség. Ezen vizsgálatok (CT, MR) csak kiújulás gyanúja esetén szükségesek.
- Tumormarkerek (CA-125, HE4) vérből történő vizsgálatának akkor van értelme, ha az korábban magas volt. Emelkedésük hónapokkal megelőzi a képalkotókkal kimutatható petefészekrák kiújulást, de az irodalmi adatok alapján ez nem jelenti feltétlenül a kiújult betegség kezelésének nagyobb eredményességét.
- Daganat kiújulásának gyanúja (panaszok, gyanús nőgyógyászati lelet, tumormarker emelkedés) esetén részletesebb képalkotó vizsgálatok (CT, MR) végzésére van szükség.
Terápiahűség: Amikor egy terápia megfelelő, akkor a betegnek is van kötelezettsége. Az, hogy betartsa az orvos utasításait, javaslatait, szedje a gyógyszert az előírtaknak megfelelően, vagy, ha laborvizsgálatokhoz, kontrollokhoz kötött a terápia, akkor azokon a megfelelő időben jelenjen meg. Ezt nevezzük terápiahűségnek.
Tudjuk, hogy a kontrollvizsgálatok lelkileg nagyon megterhelőek, de gondoljunk mindig arra, hogy jövőnk és egészségünk múlik rajta, így semmiképpen ne halogassuk azokat!
Gyógyulás
-
teljes gyógyulás: Onkológiai szempontból gyógyultnak tekintik a beteget, amennyiben 5 év után is daganatmentes. Ezért is nagyon fontos a kontrollvizsgálatok folytatása. Lásd: utánkövetés állomás.
-
krónikus állapot fenntartása: Ez azt jelenti, hogy a jelenleg rendelkezésre álló kezeléssel nem gyógyítható meg az érintett, de petefészekrák esetén számos különböző típusú kemoterápia létezik, és néha lehetőség van egy másik műtétre is, ezért mindaddig, amíg még vannak kezelési lehetőségek, képesnek kell lenni a betegséggel való együttélésre. Senki, még az orvos sem tudja, meddig, de folyamatosan új kezeléseket fejlesztenek ki.
Ne feledkezz meg a rendszeres kontrollvizsgálatokról! Minden jót kívánunk Neked!
Kiújulás

Az alábbi kezelési elvek a petefészek daganatok döntő többségét képező, hám eredetű daganatokra vonatkoznak. A ritkább, más szövettani szerkezetű tumorok kezelése ettől eltérhet.
A petefészekrák – a többi daganathoz hasonlóan – hajlamos a kiújulásra. Az esetek 60%-a 1 éven belül, az esetek 78%-a 3 éven belül jelentkezik újra.
Abban az esetben, ha az első alkalommal időben, korai stádiumban kerül felismerése, kisebb az esélye annak, hogy a betegség kezelés után (hamar) visszatér.
A kiújult daganat tünetei legtöbbször hasonlóak az első felismeréskor jelentkezőkkel.
A kiújulás során a daganat újra megjelenhet a petefészkek helyén, de a hasüregben, a nyirokcsomókban, a májban, tüdőkben, lépben, csontokban is. Ezek a gócok ugyanúgy a petefészekrák sejtjeiből állnak, annak ellenére, hogy a petefészek már eltávolításra került.
A gondozás során végzett vizsgálat (a panaszok, tünetek elemzése, fizikális vizsgálat, vérből vett tumormarkerek (CA125, CEA/, CT) célja, hogy a kiújulás időben felismerésre kerüljön, és a kiterjedése megállapítható legyen.
A kezelés lényegesen különbözik a fél éven belül és a fél éven túl kiújult daganatok esetében.
A platina tartalmú kezelés után fél éven túl kiújult betegséget „platina-érzékeny” daganatnak hívjuk. A prognózis kedvezőbb, mint a fél éven belül kiújultak esetében.
Amennyiben csak néhány áttét igazolódik, és ezek eltávolíthatóknak tűnnek, az első lépés a műtét. A műtét elvégzésének akkor van értelme, ha az összes daganatos gócot el lehet távolítani, és utána a kemoterápiát csak ún. biztosító kezelésként alkalmazzák.
Ha a gócok nem távolíthatók el (mert pl. olyan helyen van, hogy magas a műtéti szövődmény lehetősége, vagy túl sok góc van, vagy távoli helyen alakult ki: tüdőben, májban, csontban), újra a platina tartalmú kezeléshez folyamodnak.
Ha a korábbi kemoterápiás kezelés után nem maradt vissza mellékhatás (pl. kéz-láb zsibbadás), úgy ezt ismételik meg.
Ha maradt vissza mellékhatás, akkor platina-monoterápia vagy platinabázisú kombináció választható. A kezelés hatékonyságát növelhetik a kemoterápia mellé adott egyéb kezeléssel, természetesen az előnyöket és a kockázatokat mérlegre téve.
A kezelések eredményességét három ciklusonként CT és CA125 vizsgálatokkal ellenőrzik. Ha a daganatos gócok száma és mérete csökken, a kezelést folytatják. Ha úgy tűnik, hogy eltávolíthatókká váltak, a műtét lehetősége ismételten felmerül.
Ha teljesen eltűnnek a gócok, a kezelést befejezik. Ekkor szóba jöhet ún. PARP-inhibitor fenntartó kezelés, mely bizonyos molekuláris eltérések esetén (ún. BRCA-pozitív betegeknél) jelentősen megnyújtja a következő kiújulásig eltelt időt.
Ha lényeges változás nincs, a kezelés szintén folytatható, nem tolerálható mellékhatások megjelenéséig.
Ha új áttétek jelennek meg, vagy a gócok mérete jelentősen nő, terápiaváltásra van szükség. A betegséget ezek után „platina-refrakternek” tekintjük, kezelése a „platina-rezisztens” betegségnek megfelelően történik.
„Platina-rezisztens” a betegség, ha az előző (platina tartalmú) kezelés után fél éven belül újul ki. A prognózis rossz, ezért általában a műtét nem jön szóba.
Ebben az esetben platinamentes kemoterápiák közül választhatnak, melyeket önmagukban vagy az érképződést gátló kezeléssel kombinálva alkalmazhatnak. Természetesen az előnyöket és a kockázatokat itt is mérlegre téve.
A nemzetközi és a hazai terápiás javaslatok alapján, ha két egymást követő platinamentes kezelésre nem reagál a tumor, nem érdemes harmadik szert alkalmazni, mert fellépett az ún. kemorezisztencia.
Ilyenkor még a hormonterápia is szóba jöhet, ha a szövettani vizsgálat alapján a daganat erre érzékeny lehet.
Mind a platinaérzékeny, mind a rezisztens (a platina-kezelésre nem érzékeny - tehát nem működik a platina alapú kemoterápia, mint kezelés) tumorok esetében érdemes megfontolni az orvos által ajánlott klinikai vizsgálatban való részvételt, hiszen ez plusz terápiás lehetőséget jelent. Lásd: Klinikai vizsgálatok állomás
Kemorezisztencia esetén (nem használ a kemoterápia) - molekuláris patológiai elemzéssel feltárt célpontok esetében - a célzott kezelés is rendelkezésre áll.
Mivel a petefészekrákok többségét igen előrehaladott stádiumban fedezik fel, a kemoterápiás kezelés ellenére is gyakori a kiújulás (recidíva). Éppen ezért a kezelt betegeket igen szoros ellenőrzés alatt tartják, és gyakori felülvizsgálatokra van szükség.
Ez rendszeres nőgyógyászati vizsgálatot, ultrahang- és CT-vizsgálatot valamint a CA-125 tumormarker szintjének folyamatos megfigyelését jelenti.
Kiújulás gyanúja esetén szükség lehet újabb laparotómiára, azaz hasfalon keresztüli mintavételre, mert legbiztonságosabban így lehet észrevenni a visszamaradt, vagy kiújuló daganatot. Ilyet azonban egyre ritkábban végeznek, mert a korszerű diagnosztikai eszközök segítségével egyébként is megbízható felvilágosítás nyerhető a daganat esetleges kiújulásáról.
Onkológiai Centrumok, melyekkel a Mályvavirág Alapítvány együtt dolgozik:
Budapest
Debrecen
Mályvavirágok Közössége a Facebookon - titkos és zárt csoport:
Nőgyógyászati daganattal érintettek csoportja. A tagok beszélgetnek, információkat osztanak meg, kérdeznek, tanácsolnak, segítik egymást. A csoportban szakemberek is jelen vannak, moderált, szabályzattal ellátott közösség a Facebookon.
Itt mindenről szó van, jó és rossz dolgokról is. Lehet aktívan részt venni benne és hátulról figyelni. Ki lehet menni bármikor és újra kérni a felvételt.
Titkos és zárt, nem látszik az adatlapon, ha csatlakozol, és megtalálni sem lehet.
Csoportba bejutás:
1. lépés, hogy like-old a Mályvavirág nyílt oldalt, ha még nem tetted meg,- csak így tudunk a zárt csoportba tenni.
2. lépés: kérjük töltsd ki ezt a kérdőívet: https://forms.gle/uvf6tasEVrpf7j4K6
3. lépés: Facebook értesítés érkezik neked, hogy bejöhetsz a csoportba.
Amennyiben elakadnál, kérjük, vedd fel velünk a kapcsolatot: infoinfo [at] malyvavirag.humalyvavirag.hu
Tóth Icó: Libellus - Minden anyuka meggyógyul! - igényelhető a Mályvavirág Alapítványtól
Nőgyógyászati daganatok kiújulása
Lelkemnek - foglalkoztatófüzet (az ingyenes kiadványt a kórházban vagy kérd az info [at] malyvavirag.hu e-mail címen)
Mályvaspájz - dietetikai könyv
Műtét / kiújuláskor

Kiújulás esetén legalább fél-1 évnek el kell telnie a kemoterápiát követően, aztán kerül sor a műtéti kezelésre. Amennyiben az utolsó kemoterápia időpontja engedi, a kiújulás pontját megkeresve, célzottan történik az operáció.
HIPEC: ennek angol jelentése: Hyperthermic intraperitoneal chemotherapy. Egyszerre alkalmazzák a kemoterápiás kezelést a műtéttel kombinálva, előrehaladott hasi daganatok kezelésében. Felmelegített rákellenes gyógyszereket infúzióval adnak be, és rövid ideig keringetnek a hasüregben.
A kemoterápiás gyógyszereket körülbelül 106-109 °C-ra melegítik. A rákos sejtek nem képesek kezelni a hőt, ahogy egyébként az egészséges sejtek sem. A hő segít abban is, hogy a gyógyszerek könnyebben belépjenek a sejtjeidbe.
A HIPEC nagy műtét, amely 8-10 óráig, vagy még hosszabban tart, altatásban végzik. Először a sebész eltávolít minden látható daganatot. Ezt a lépést nevezzük citoreduktív műtétnek vagy “CRS”-nek. Ezután a hasban felmelegített kemoterápiás gyógyszereket keringetnek.
Orvosod a te egyedi körülményeid alapján dönt a gyógyszerek pontos kombinációjáról és a testben maradás időtartamáról. A legtöbb esetben a HIPEC 30-120 percig tart. Az egészségügyi csapat ide-oda ringat, hogy megbizonyosodjon arról, hogy a gyógyszerek minden zugba eljutnak. Annak érdekében, hogy a test belső hőmérséklete ez idő alatt alacsony maradjon, egy speciális hűtőtakaróra tesznek. A HIPEC nem jelent minden petefészekdaganatos beteg számára megoldást, a módszer szükségességét szuperspecializált szakemberek csoportjának véleménye alapján érdemes eldönteni.
Ha elegendő idő telik el, a gyógyszerek kiürülnek a hasadból, megtörténik annak összevarrása, majd az intenzív osztályon maradsz egy ideig megfigyelésen.
AZ ALTATÁS

Mi is az az anesztézia?
A szó jelentése érzésnélküliség, vagyis arra szolgál, hogy a fájdalmas vizsgálat vagy műtéti beavatkozás alatt kikapcsolja azokat a jelzéseket, amik a fájdalom érzését juttatják el az agyunkba.
Az anesztézia lehet általános = altatás, ilyenkor alszol, és semmit nem érzel, érzékelsz a külvilágból, vagy regionális = ilyenkor a testnek egy részét kapcsolják ki az érzések közvetítéséből, ilyen a spinális, epidurális, regionális és a helyi érzéstelenítés.
Mit csinál az aneszteziológus?
- veled egyetértésben megtervezi a műtéthez szükséges érzéstelenítést,
- ellenőrzi az életfunkciókat a műtét/altatás alatt,
- adagolja a gyógyszereket, altatógázokat, szükség esetén antibiotikumokat vagy vérkészítményeket,
- megtervezi a műtét utáni fájdalomcsillapítást,
- felügyeli a műtét utáni állapotodat az őrzőben vagy az intenzív osztályon.
Mik a teendők műtét/ altatás előtt?
- ha dohányzol, minél hamarabb hagyd abba, legjobb hetekkel a tervezett műtét előtt,
- a túlsúly fokozott műtéti rizikót jelent, ha lehet egy könnyű diétával hozd formába magad,
- ha van mozgó vagy törött fogad, keresd fel a fogorvosodat,
- ha van krónikus alapbetegséged, menj el a gondozó orvosodhoz, hogy a lehető legjobb állapotba kerülj a műtét időpontjára.
Mi az az aneszteziológiai ambulancia?
A műtét előtt találkozni fogsz egy aneszteziológussal, aki előzetes felmérést fog végezni az állapotodról, és megbeszélhetsz vele minden részletet az altatással kapcsolatban. Az aneszteziológiai ambulancián a háziorvosi vizsgálathoz hasonló vizsgálat történik, kikérdeznek, megmérik a vérnyomásodat, megnézik a leleteidet. Szinte minden esetben szükséges egy EKG és egy laborvizsgálat műtét előtt, de lehet, hogy egyéb eredményekre is szükség lesz, pl. mellkas röntgen, esetleg szívultrahang, ezt az aneszteziológus dönti el.
Mi történik a műtét előtt, alatt, után?
A műtét előtt már az előző napon valószínűleg be kell feküdni a kórházba. Sok helyen már vacsorázni sem lehet a műtét előtti napon, sőt lehet, hogy beöntést vagy hashajtót fogsz kapni. Erre azért van szükség, hogy kiürüljenek a belek, jobb műtéti körülményeket teremtve. Figyelj a folyadékbevitelre, inni a műtét előtt maximum 2 órával még lehet, vizet, teát vagy szűrt gyümölcslevet, igyál eleget!
Már este is, de a műtét reggelén biztosan fogsz kapni egy „bátorító tablettát”, ez segít, hogy könnyebben átvészeld a műtét előtti várakozást.
És amikor eljön az idő, jön érted a műtősfiú! Le kell majd vetkőzni teljesen, lehet, hogy kapsz egy kórházi hálóinget, de az is lehet, hogy csak jól betakarnak. A műtőben kapsz egy sapkát, ellenőrzik a személyazonosságodat, a csuklódon lévő kis névjegykártyát, egyeztetik a műtét típusát.
Aztán előkészítenek az altatáshoz: EKG-tappancsokat raknak a mellkasodra, vénát biztosítanak, vérnyomásmérőt helyeznek a felkarodra, ami 5 percenként mérni fog, az ujjad hegyére pedig kapsz egy kis csipeszt, ami a vér oxigénszintjét fogja mérni.
Ha epidurális kanült beszéltetek meg, azt ebben a fázisban teszik be. Fel kell majd ülnöd, kapsz egy kis helyi érzéstelenítőt a szúrás helyére, és két csigolya között bevezetik ezt a kis csövecskét, amin keresztül műtét után kaphatsz majd fájdalomcsillapítót.
Ezután jön az altatás: kapsz majd fájdalomcsillapítót, altatószert, és, ha már mélyen elaludtál, izomlazítót is, hogy a lélegeztető csövet be tudják helyezni a légcsövedbe. A műtét alatt az aneszteziológus minden életfontos paramétert folyamatosan ellenőrizni fog, ha szükséges, ad még gyógyszert, irányítja a lélegeztetést, folyadékot pótol, mindent megtesz azért, hogy a lehető legjobban bírd a műtétet.
Amikor a sebész befejezte, leállítják a gyógyszerek és altatógázok adagolását, és hagyják, hogy magadtól felébredj. Ébredés után még kába leszel, nem fogsz emlékezni rá, de átkerülsz majd az őrzőbe, ahol még rendszeresen mérik az életfontos paramétereket, lesz rajtad egy oxigénmaszk, és egy szakképzett nővér felügyeli a fájdalomcsillapítást. A hasadból valószínűleg drének lógnak majd ki, kötés lesz rajta, és szinte biztos, hogy hólyagkatétered lesz. Nyugi, semmit nem viszel haza, ezeket mind szépen fokozatosan eltávolítják majd, de most segítenek.
Az osztályra vissza:
Mikor már minden értéked stabil, és a fájdalom is jól kontrollálható, visszakerülsz a „sima” osztályra. A műtét típusától függ, hogy mikor, de lassan elkezdhetsz kortyolni folyadékot, később ehetsz is pár falatot, szigorúan az előírt diétás szabályok szerint. Ne felejtsd, az egész hasadat megbolygatták, idő kell a beleknek, hogy magukhoz térjenek. Jön majd gyógytornász, lehet, hogy pszichológus, és persze a kezelőorvosod is elmondja majd a műtét menetét.
Lehet az altatásnak szövődménye?
Lehet. Minden orvosi beavatkozásnak lehetnek mellékhatásai és szövődményei, még akkor is, ha mindent elkövetnek, hogy ne legyen. A leggyakoribb mellékhatások: rossz közérzet, szédülés, hányinger, aluszékonyság, fejfájás, ezek rövid idő alatt maguktól is megszűnnek.
Az altatás leggyakoribb szövődménye a torokfájdalom (a lélegeztetőcső miatt) illetve fogsérülés (ez pedig a lélegeztetőcső behelyezésekor alakulhat ki). Ritkán előfordulhat vérnyomásingadozás, szívritmuszavar, szívelégtelenség, allergiás reakció gyógyszerekre, műtét utáni légzési nehézség, ezekre az altatóorvos előre figyelmeztetni fog, ha a műtét jellege vagy az alapbetegségeid miatt fokozott kockázatnak vagy kitéve.
Mályvavirág Szakmai Bizottság
A Mályvavirág Alapítvány szorosan együttműködik egészségügyi szakemberekkel - legyen szó akár egy kiadvány elkészítéséről, diagnózis felállításáról, vagy műtétekről, terápiákról, másodvéleményről, intézményi együttműködésről, felvilágosító munkáról, információ szerzésről vagy átadásról.
Keresd bizalommal őket!
https://malyvavirag.hu/szakmai-bizottsag
Mályvavirágok Közössége a Facebookon - titkos és zárt csoport:
Nőgyógyászati daganattal érintettek csoportja. A tagok beszélgetnek, információkat osztanak meg, kérdeznek, tanácsolnak, segítik egymást. A csoportban szakemberek is jelen vannak, moderált, szabályzattal ellátott közösség a Facebookon.
Itt mindenről szó van, jó és rossz dolgokról is. Lehet aktívan részt venni benne és hátulról figyelni. Ki lehet menni bármikor és újra kérni a felvételt.
Titkos és zárt, nem látszik az adatlapon, ha csatlakozol, és megtalálni sem lehet.
Csoportba bejutás:
1. lépés, hogy like-old a Mályvavirág nyílt oldalt, ha még nem tetted meg,- csak így tudunk a zárt csoportba tenni.
2. lépés: kérjük töltsd ki ezt a kérdőívet: https://forms.gle/uvf6tasEVrpf7j4K6
3. lépés: Facebook értesítés érkezik neked, hogy bejöhetsz a csoportba.
Amennyiben elakadnál, kérjük, vedd fel velünk a kapcsolatot: infoinfo [at] malyvavirag.humalyvavirag.hu
Lelkemnek - foglalkoztatófüzet (az ingyenes kiadványt a kórházban vagy kérd az info [at] malyvavirag.hu e-mail címen)
Sugárterápia / kiújuláskor
SUGÁRKEZELÉS=RADIOTERÁPIA
A sugárkezelés a daganatos elváltozás egyfajta kezelési lehetőségét jelenti, amely leggyakrabban röntgensugarakat, olykor radioaktív forrásokat használ. Az itt használt röntgensugarak erősebbek, mint a hagyományos diagnosztikai célú röntgensugarak. A sugárkezelés tehát a rák gyógyítását, a daganat növekedésénék gátlását, csökkentését, vagy a fájdalom enyhítését szolgálja.
Sugárkezelés fajtái:
- Külső sugárkezelés (EBRT—External Beam Radiation Therapy)
- Belső sugárkezelés, közelterápia = Brachyterápia ( HDR-AL- High Dose Rate)
A petefészekdaganatok korszerű ellátásában elsődleges szerepe a műtétnek van. Az igen jó terápiás hatékonyságú platina-taxán alapú kemoterápiás szerek mellett a sugárkezelések háttérbe szorultak. Ennek fő oka, hogy ilyen esetekben a sugárterápia céltérfogata a teljes hasűr, azonban itt rengeteg kritikus, sugárérzékeny szervünk található (belek, vese, stb). Emiatt magas dózis nem adható még a legkorszerűbb technikák (képvezérelt-intenzitásmodulált sugárkezelés) igénybevételével sem, ellenben súlyos mellékhatások alakulhatnak ki. A petefészekdaganatok műtét utáni sugárkezelésére a mai napig nem állnak rendelkezésre magas szintű tudományos bizonyítékok. Amennyiben mégis úgy döntünk, hogy megkíséreljük a sugárkezelést, két lehetőségünk adódik:
1, a hasüregbe fecskendezett izotóp anyagokkal, amennyiben kisméretű, néhány mm-es vagy kisebb ún. mikroszkópikus daganatszóródást feltételezünk. A műtét után 1-2 héttel, infúziós oldatban arany, vagy krómfoszfát izotópot juttatunk a hasűrbe, előre meghatározott ideig. Bélösszenövés gyanúja esetén azonban ezt a módszert tilos alkalmazni, ugyanis a letokolt belekbe az összenövések mentén az izotóp bezáródhat, súlyos bélelhalást okozva.
2, külső sugárkezeléssel: ilyenkor egy nagyméretű készülék végzi el a céltérfogat besugárzását, számítógépes tervezést követően. A kezelés fájdalmatlan, a gyorsító készülék kezelő asztalán, hanyatt fekvő pozícióban történik, napi rendszerességgel (hétfő-péntek), 3-6 hét hosszan. A lehetséges mellékhatások a besugárzás alatt, vagy az azt követő napokban jelentkeznek: hasmenés, puffadás, teltségérzet, émelygés, hányinger, súlyosabb esetekben hányás is előfordulhat. Amennyiben kemoterápia előzte meg a sugárkezelést, úgy a mellékhatások súlyossága is fokozódhat.
Nagyméretű daganatok esetén egyik módszertől sem várható a daganat teljes elpusztítása, ilyenkor ún. palliatív sugárkezelést alkalmazunk, azaz a célunk a daganat okozta tünetek, panaszok enyhítése (fájdalom, vérzés), és nem a daganatmentesség elérése. A palliatív kezelések 1-2 hétig tartanak, szintén napi rendszerességgel. A mellékhatások enyhébbek lehetnek, a csökkentett összdózis miatt. A palliatív kezelések egy speciális fajtája a hüvelyen keresztül történő ún. brachyterápia. Ebben az esetben a hüvelyben, vagy hüvelycsonkban elhelyezkedő daganatot vagy áttétet próbáljuk meg elpusztítani, vagy a vérzéses panaszt csökkenteni. Ezek a kezelések heti rendszerességgel történnek, és összesen 3-6 alkalomra lehet szükség a kívánt cél eléréséhez. Tekintve, hogy ilyenkor csak a hüvelyfal 5-6 mm-es rétegét kezeljük, a környező szervek minimális sugárterhelést szenvednek, így a külső sugárkezeléskor várható mellékhatások itt enyhébbek, vagy egyáltalán nem jelentkeznek.
Sugárterápiás szakember, szakorvos - Onkológiai Intézményekben, centrumokban
Kemoterápia / Kiújuláskor

Kemoterápiás szereknek nevezzük azokat a gyógyszereket, melyek hatásmechanizmusuk során károsítják a szervezet osztódó sejtjeit. Ezek a gyógyszerek ugyan minden sejtünkre hatnak, azonban lényegesen kisebb fokban károsítják a normál sejteket, mint a daganatosokat, amelyekkel szemben harcolnak. A kezelés során elpusztul az összes éppen osztódó sejt, azonban a kezelés utáni időszakban az egészséges sejtek az eredeti, normális mennyiségre szaporodnak, míg a daganatsejtekből kevesebb lesz és számuk lassabban emelkedik a kiindulási értékhez képest.
A kezelés célja a daganatos beteg teljes gyógyulása, a daganatmentes időszak elérése, vagy ennek elmaradása esetén a daganat növekedésének lassítása, leállítása. Meg kell jegyeznünk azt is, hogy olykor csak a tünetek enyhítésére van lehetőségünk.
Kemoterápia csak a daganat szövettani típusának tisztázását követően, szakbizottsági döntésnek megfelelően adható, hiszen minden kezelést szerv- és szövetspecifikusan választanak ki az orvosok. A kezelési tervet az onkológus állítja fel, ez mindig az adott esettől és a kezelések hatékonyságától függ. A kemoterápiát minden alkalommal a páciensre dozírozzák (adagolják) testfelszín vagy speciális logaritmus alapján.
A kemoterápiának bizony vannak mellékhatásai. Mint minden gyógyszerkészítményre, a kemoterápiára is lehet allergiás a páciens. Sajnos a tenyérviszketéstől, a kipirosodástól a nehézlégzésen, a szívdobogásérzésen, a deréktáji fájdalmon át, a súlyos anafilaxiás reakciókig bármi előfordulhat, azonban szakképzett személyzet áll rendelkezésre, akik ezeket a reakciókat azonnal kezelni tudják.
Amennyiben a beteg rosszul tolerálja a kezelést, a panasz súlyosságától függően akár a kemoterápiás készítmény változtatására is sor kerülhet. A panaszok enyhítésére, kivédésére a kezelés előtt előkészítő gyógyszereket alkalmaznak, melyek gondoskodnak a gyomor védeleméről, illetve allergia elleni antihisztamint, szteroidot és hányáscsillapító gyógyszert is kap a beteg. Számítani kell arra is, hogy a páciens otthonában további mellékhatások várhatóak. A hányinger, a hányás, a hasmenés és a székrekedés gyakori panasz. Vannak készítmények, melyek alkalmazása a bőr, a haj és a köröm állapotát is érintik, mint a haj elvesztése, vagy a körmök elszíneződése, gombásodása. Nyálkahártya gyulladás, szájszárazság is jelentkezhet. A vérsejteket érintő mellékhatások fokozódnak a felvett kemoterápiák számával, így csökkent fehérvérsejt, vörösvérsejt és vérlemezke számot mutatnak a laborvizsgálatok eredményei. A kemoterápia és a daganat maga is fokozza a trombóziskészséget ( vérrögképződés), így az orvosok vérhígító készítményt alkalmaznak ennek megelőzésére.
Szívizomkárosodás a kardiotoxikus készítmények esetében várható, így szívultrahang vizsgálattal figyelemmel kísérjük a szív pumpafunkcióját, hiszen csak adott határérték felett adhatóak ezek a készítmények. Vannak olyan gyógyszerek, melyek a perifériás idegeket bántják, így a talp- és az ujjbegyek zsibbadását okozzák. Máj- és vesefunkciós eltérések abból adódhatnak, hogy a kemoterápiás hatóanyagok vagy a májon vagy a vesén keresztül választódnak ki.
A kemoterápia menete
Minden kezeléssorozat egy megbeszéléssel indul, ahol az orvos és a beteg meghatározzák a célt, és megtervezik a kezeléseket. Megbeszélik, hogy milyen mellékhatások várhatók, és minden felmerülő kérdésre választ adnak. Szó esik arról is, hogy a megfelelő táplálkozással hogyan védhetünk ki bizonyos panaszokat, és mivel segíthető még a gyógyulás. Ilyenkor felírják az előkészítő gyógyszereket is, és megbeszélik az adagolásukat. A kezelésekre reggel kell érkezni, mert a gyógyszer vénás infúziós beadása órákat vehet igénybe, de a jó hír, hogy még aznap haza is mehetnek a betegek. Az első kezeléskor beleegyező nyilatkozatot kell a páciensnek aláírnia, esetenként a szívultrahang eredmény is szükséges. Minden kezelés előtt friss laborvizsgálatot végeznek, mely tartalmazza a vérképet, máj- és vesefunkciós paramétereket, ionokat, vizeletvizsgálatot. Amennyiben ezek megfelelőek a kezeléshez, súlymérést követően kiszámolják a kemoterápia dózisát. A betegnek ilyenkor lehetősége van arra, hogy megbeszélje a panaszait orvosával, és megoldást keressenek rá. Ezek után a kezelési lappal a kemoterápiás kezelőbe irányítják a beteget, ahol a gyógyszertárból megrendelt gyógyszer megérkezését követően a nővér beköti az előírt készítményt, amennyiben a beteg vitális paraméterei rendben vannak. A kezelő helyiségek jól felszereltek a beteg ellátására és kényelméhez igazodva.
Amennyiben zavartalanul lefolyt a kezelés, a beteg kézhez kapja az ambuláns lapját, a beutalót, a receptjeit, és otthonába távozhat. Kezelést követően 1 héttel vérkép laborvizsgálat szükséges, annak ellenőrzésére, hogy a kemoterápia milyen mértékben károsította a csontvelőt, és amennyiben szükséges, lehetőség van a csontvelő támogatására.
Kóros értékek: fehérvérsejtszám 2,0 G/l alatt; abszolút neutrofil szám 1,5 G/l alatt; hemoglobin 9,0 g/dl alatt; vérlemezke 100 G/l alatt. A mellékhatások a kezelést követő másod-harmadnap jelentkeznek változó intenzitással. A páciensek a megbeszélteknek megfelelően járnak el a mellékhatások megjelenésekor, de olykor előfordul, hogy orvosi segítségre van szükségük ezek megoldására, ilyenkor az egészségügyi személyzet a betegek rendelkezésére áll a megadott elérhetőségeken.
A kezelések hatékonyságát képalkotó vizsgálattal, bizonyos tumorok esetén tumormarkerrel követik. Amennyiben rezisztencia alakul ki egy készítménnyel szemben, vagyis a tumor nem reagál megfelelően a kezelésre, terápiaváltásra kényszerülnek, ezzel kapcsolatban az orvos kimerítő tájékoztatást fog adni betegének.
Többedvonalbeli kezelés: rezisztencia miatt gyógyszerváltást követően adott gyógyszer, mely tumormentességig vagy rezisztenciáig, a daganatos betegség rosszabbodásáig adható.
PARÓKA/KENDŐ:
Paróka:
A parókát/kendőt bizonyos kezelések mellé felírják receptre, így kedvezményesebb áron lehet hozzájutni. A receptet már az első kezelés alkalmával megkapják a betegek, és maguk választanak üzletet és parókát. A kedvezmény mértéke üzletenként eltérő lehet. Érdemes az első kezelést követően parókákat próbálni, mert általában az első kezelést követő 10-14. napon szinte a teljes hajkoronát elveszti a páciens. A parókát értékesítő üzletekben nagyon tapintatosak és segítőkészek az alkalmazottak. Érdemes több fazont is próbálni, hogy kialakuljon, melyik a legkomfortosabb viselet számunkra. Azzal is számolni kell, hogy a paróka próbálásakor még megvan a hajunk, viszont amikor már viseljük magát a parókát, nem lesz olyan hajtömeg alatta. A paróka alá - hogy ne irritálja a fejbőrt - lehet nylon harisnya anyagból készült kis sapkát venni.
Van igazi hajból készült és műhajból készült paróka. A műhajból készült paróka ápolása nagy odafigyelést igényel: extrém hőhatásnak nem szabad kitenni, hajszárítóval és hajvasalóval általában nem formálható, azonban speciális készítményekkel mosható. A paróka fazonját megtartja mindenféle formázás nélkül is a mosást követően. A valódi hajból készült paróka ápolása nagyon hasonlít a saját hajunk ápolásához.
Kendő:
A paróka mellett/helyett lehetőség van kendő viselésére is. Ebből is többféle megoldás létezik. Vannak előre gyártott kendők, amiket csak mint egy “sapka” kell felvenni, és esetleg hátul a tarkónál megkötni. Általában puha pamut anyagból, esetleg öko-pamutból készülnek, hogy a kopasz fejbőrön kényelmes viseletet adjanak. Nagyon komfortos viselet, akár többféle szín és fazon is beszerezhető, így változatosabbá tehető az öltözködésünk. Az előre megvarrt kendők mellett nagyon praktikus a normál női kendők/sálak viselése is. Ezek általában téglalap alakú, hosszú kendők, amikkel megfelelő kötési technikával olyan végeredményt érhetünk el, mint egy előre megvarrt kendővel. Ezek lehetnek pamutból vagy selyemből, esetleg keverék anyagból készült vékony sálak is. Nagyon komfortos a viselésük.
Turbán:
A kendők mellett lehet a paróka árusító üzletekben ún. turbánokat is vásárolni. Ezek általában - évszaknak megfelelően - vastagabb vagy vékonyabb pamutból készült kis “sapkák”, némi rafinériával megvarrva. Nagyon egyszerű a viselésük, mert tényleg, csak, mint egy sapkát kell felvennünk.
Mi szól mellette és ellene?
Paróka
Mellette:
- egy jól megválasztott fazon esetében kívülálló számára szinte észrevehetetlen, úgy tudjuk viselni, mint a saját hajunkat
- nem igényel napi fazon beállítást
- könnyű kezelés
- bizonyos munkakörökben, vagy, ha nem szeretnénk a környezetünk tudomására juttatni betegségünket egy optimális megoldás
- szinte mindenféle tevékenység végezhető vele, akár sportolás is
- recepttel támogatott a vásárlása
Ellene:
- melegebb viselet
- nehéz az eredeti hajszínünkhöz és formánkhoz nagyon hasonlót találni
- speciális eszközöket igényel az ápolása
- megosztóbb a viselése
- nem mindenki tudja elviselni a fejbőrén a parókát
- “idegen érzés” a tükörbe nézve
Kendő
Mellette:
- nagyon komfortos viselet
- többféle kendővel változatosabbá tehetjük az öltözködésünket
- nem meleg a nyári napokban sem
- olcsóbban beszerezhető
- a kezelések befejeztével is tovább hordható sálként/női kendőként, mint a sziluettünk része
- szépen kiemeli az arc vonásait
- mindenféle tevékenység végezhető benne
- nem igényel kifejezett ápolást, mosható, gyorsan szárad
- könnyen variálható
Ellene:
- egyértelműsíti a betegségünket
- támogatás nem kérhető rá
- picivel több időt igényel a felkötése (kivéve, ha előre varrt kendőről van szó)
- a fület eltakarja, ami zavaró lehet
Védeni kell a napsugárzástól a bőrt, mert a citosztatikumok fényérzékenyek, és hamarabb bomlanak le fény hatására a szervezetünkben.
FONTOS:
A nőgyógyászati daganatok kezelése onkológiai centrumban történjen, erre a területre specializálódott nőgyógyász onkológus, klinikai onkológus, daganatsebész által!
GÉNVIZSGÁLAT/Kiújuláskor
Molekuláris patológiai vizsgálat
Ezek olyan vizsgálatok, amelyek előre jelezhetik, hogy az adott daganatra milyen gyógyszer lehet hatásos. Azt vizsgálják, hogy van-e mutáció a génekben, ha igen, akkor ezek meghatározásra kerülnek, majd az eredmények függvényében megállapítható, hogy van-e olyan kezelés, ami a betegnek segíthet a gyógyulásban, vagy az élet meghosszabbításban. Szekvenálásnak hívjuk a daganatsejtek felépítésének, mutációinak kimutatását, a daganatsejtek elemzését. Nagyon költséges eljárás. Fontos hangsúlyozni, hogy azokat a molekuláris génvizsgálatotokat, melyek a kezelést befolyásolják, vagy amelyek jelenlétében van gyógyszeres kezelési lehetőség, specializált daganatközpontban, államilag finanszírozva is el lehet érni.
Géntérkép

Az emberi géntérkép elkészítése áttörést hozott az orvostudományban. Azon túl, hogy megismertük az emberi genomot, új utakat nyitott meg a betegségek genetikai eredetének feltérképezésére. Ma már nem csak ritka genetikai betegségeket lehet vizsgálni ezekkel a módszerekkel, géntérképünk többek között azt is megmutatja, hogy hordozunk-e olyan mutációkat, amelyek betegségeket okoznak, illetve hogy van-e olyan eltérés, amely segít a betegség kezelésében. Sajnos kevesebb a terápia, mint a kimutatott mutációk, de a teljes géntérkép megismerése segíti a tudomány fejlődését, új lehetőségek feltárását, rengeteg adatot szolgáltat.
A teljes géntérkép elkészítése nagyon költséges, és csak kivételes esetben támogatja a biztosító. A daganatos betegségek diagnosztikájában ugyanakkor egyre nagyobb szerepet kapnak a molekuláris genetikai vizsgálatok, amelyek a daganat jellemzőinek részletes feltérképezése révén hatékony, egyénre szabott kezelést tesznek lehetővé. Fontos hangsúlyozni, hogy azokat a molekuláris génvizsgálatotokat, melyek a kezelést befolyásolják, vagy amelyek jelenlétében van gyógyszeres kezelési lehetőség, specializált daganatközpontban, államilag finanszírozva is el lehet érni.
BRCA

A BRCA a Breast Cancer Antigen angol rövidítése, ami mellrákot jelent. Elsőként az emlőrák kapcsán ismerték fel, innen jött az elnevezés. Ezek a gének minden emberben megtalálhatóak.
A BRCA1 és BRCA2 gének olyan fehérjéket kódolnak, amelyeknek az a feladata, hogy segítsenek a sejtben létrejövő DNS-károsodások javításában, és így biztosítsák a sejtek normális működését. Előfordul, hogy valamelyik BRCA-gén működése meghibásodik (ezt nevezzük mutációnak), emiatt a DNS-hibajavítás nem működik megfelelően, ami daganatképződéshez vezethet. A mutáció megjelenhet csak a daganatszövetben – ez nem öröklődik, vagy a test valamennyi sejtjében - ilyenkor örökletes BRCA-mutációról beszélünk.
Ez a mutáns gén generációkon keresztül öröklődhet, és elsősorban az emlőrák és a petefészekrák kialakulására hajlamosít, de egyéb daganattípusokban is szerepet játszik, pl. prosztatarák, hasnyálmirigyrák.
Fontos tudni, hogy nem minden petefészekrák, illetve emlőrák hátterében áll BRCA-mutáció.
BRCA jelentősége
-
Ha a családban halmozottan fordult elő emlőrák, petefészekrák, hasnyálmirigy vagy prosztatarák, különösen fiatal korban, akkor érdemes megnézetni a BRCA-mutációt, mert ez öröklődhet. A vizsgálat vérből történik, és genetikai tanácsadás előzi meg. Ha igazolódik a mutáció, szakorvosi konzultációt folytatnak le, hogy az emlő- és petefészekrák kialakulásának kockázatát csökkenteni tudják, illetve időben felismerjék, ha daganat alakul ki. Erre térítésmentesen az Országos Onkológiai Intézetben (Budapest), a Semmelweis Egyetemen (Budapest), a SZTE Klinikai Központban (Szeged) van lehetőség. Ezek mellett magánúton is elérhető a tanácsadás és a BRCA-tesztelés.
-
Ha már kialakult a petefészekrák, a terápiaválasztás miatt fontos tudni, hogy fennáll-e a BRCA-mutáció, mert befolyásolja a terápiát, új lehetőségeket nyit meg. Személyre szabott terápia, ún. fenntartó terápia adható a BRCA 1, 2 mutáció-pozitív betegeknek. Ilyenkor a daganatból célszerű elvégezni a vizsgálatot, erre több intézetben van lehetőség. Ezt a kezelőorvos (onkológus) kérheti meg.
HRD - Homologous recombination deficiency, homológ rekombinációs deficiencia

A DNS-hibajavítás a sejtekben állandóan zajló folyamat, amely elengedhetetlen a túléléshez. DNS-károsodást okozhatnak az anyagcsere-folyamatokból származó melléktermékek (reaktív oxigéngyökök) és külső környezeti tényezők, például UV-sugarak, egyéb sugárzás, szintetikus vegyszerek, toxinok stb., amelyek következtében naponta több százezer molekuláris károsodás alakul ki egy-egy sejtben. Ezek a károsodások roncsolják a DNS szerkezetét, így megváltoztathatják a génekben kódolt információk olvasását, javításukra szolgáló mechanizmusok folyamatosan működnek. A DNS kettős spirál szerkezetét ért károsodás típusától függően többféle javítási stratégia létezik.
Amikor a kromoszóma két szála közül csak az egyik hibás, a másik szál használható mintaként, ami alapján megtörténhet a károsodott szál javítása. Az egyszálú törések javítására szolgálnak például a kivágó mechanizmusok, amelyek eltávolítják a károsodott nukleotidot (a DNS építő egysége), és a helyére egy sértetlent építenek be úgy, hogy a másik DNS szál nukleotidját kiegészítse. Ilyen a báziskivágó javítás, amely egyetlen károsodott nukleotidot javít ki. A nukleotidkivágó javítás 2‒30 nukleotid hosszúságú károsodott szakaszokat, az össze nem illő párok javítja ki (mismatch repair), valamint a DNS megkettőződése és az azt követő rekombináció során keletkező hibás nukleotidpárokat.
Kettősszálú törés esetén a javítás két fontos mechanizmusa: a nem homológ végek összekapcsolása illetve az ún. homológ rekombinációs javítás. A rekombinációs javító mechanizmus túlnyomórészt a sejtciklus azon fázisaiban működik, amelyekben a DNS megkettőződik, vagy már megkettőződött. Az emberi genomban sok gén több példányban van jelen, így az azonos szekvenciák (gének sorrendje) több forrásból elérhetők. Az ilyen másolatokra hagyatkozó rekombinációs javítás azonban kromoszomális átrendeződésekhez vezet.
A „nem homológ végek összekapcsolása” során a törés két vége szekvencia-minta nélkül kapcsolódik össze, gyakran DNS-szekvenciák vesznek el, így ez a javítás mutációt is okozhat.
A daganatos sejtekben, amelyekben hiányoznak a hatékony homológ rekombinációs javítás alapvető funkcionális összetevői, mint például a BRCA1/2, vagy az egyéb, úgynevezett HRR-ben (homológ rekombinációs repair, azaz javítás) szerepet játszó gének, a DNS kettős spirál törések nem tudnak pontosan vagy hatékonyan kijavítódni, ami jelentős homológ rekombináció hiányhoz (HRD: homológ rekombinációs deficiencia) vezet. Ilyenkor az alternatív és „hibahalmozó” útvonalak aktiválódnak, mint például a „nem homológ vég-a-véghez illesztés”, ami a genom nagyfokú instabilitásához vezet. A DNS megkettőződési ciklusok során ez az instabilitás fokozódik.
A HRD (homológ rekombinációs deficiencia) és a kialakuló genom instabilitás különböző elváltozások ill. nagy átrendeződések formájában jelenik meg a kromoszómán. Ezen elváltozások, az ún. genomikai „hegek” kimutathatóak, és ezek alapján, meghatározott kritériumok szerint egy összetett pontszám számolható ki. Bizonyos HRD-pontszámok magában foglalják a BRCA1/2 gének mutációját és/vagy a genomikai instabilitást, így egy határérték segítségével megállapítható a HRD-pozitivitás. A BRCA- ill. HRD-státusz, valamint a platina-érzékenység (platina-alapú kemoterápiára adott megfelelő válasz) fontos előrejelző tényezője a petefészekrák fenntartó kezelésében alkalmazott ún. PARP-inhibitorok hatásosságának.
Mályvavirágok Közössége a Facebookon - titkos és zárt csoport:
Nőgyógyászati daganattal érintettek csoportja. A tagok beszélgetnek, információkat osztanak meg, kérdeznek, tanácsolnak, segítik egymást. A csoportban szakemberek is jelen vannak, moderált, szabályzattal ellátott közösség a Facebookon.
Itt mindenről szó van, jó és rossz dolgokról is. Lehet aktívan részt venni benne és hátulról figyelni. Ki lehet menni bármikor és újra kérni a felvételt.
Titkos és zárt, nem látszik az adatlapon, ha csatlakozol, és megtalálni sem lehet.
Csoportba bejutás:
1. lépés, hogy like-old a Mályvavirág nyílt oldalt, ha még nem tetted meg,- csak így tudunk a zárt csoportba tenni.
2. lépés: kérjük töltsd ki ezt a kérdőívet: https://forms.gle/uvf6tasEVrpf7j4K6
3. lépés: Facebook értesítés érkezik neked, hogy bejöhetsz a csoportba.
Amennyiben elakadnál, kérjük, vedd fel velünk a kapcsolatot: infoinfo [at] malyvavirag.humalyvavirag.hu
Titkos és zárt Facebook csoport a terápia témában:
https://www.facebook.com/groups/360804698536521/member-request
A linkek eléréséhez kattints a címekre!
Célzott terápiát támogató molekuláris onkológiai innováció a Semmelweis Egyetemen
Tóth Icó: Libellus - Minden anyuka meggyógyul! - igényelhető a Mályvavirág Alapítványtól
Fenntartó terápia / Kiújuláskor

Olyan daganatellenes kezelés, amelynek célja, hogy folyamatos alkalmazásával megakadályozza a primer daganat kiújulását, vagy lelassítsa a daganat növekedését. A fenntartó kezelést a betegség progressziójáig, vagy elfogadhatatlan mértékű mellékhatások megjelenéséig alkalmazzuk. A nőgyógyászati daganatok esetében több fajta fenntartó kezelés is létezik, ilyenek pl. az érképződést gátló, a PARP-gátló kezelések vagy az immunterápia. A fenntartó kezelések nem minden nőgyógyászati daganatos betegségben érhetőek el, s adott betegségen belül is vannak olyan előre meghatározott betegcsoportok, akik számára ez a kezelés előnyt jelenthet, mint pl. a BRCA-mutációt hordozó, bizonyos szövettani típussal rendelkező petefészekrákos nők esetében a PARP-gátlók alkalmazása. Kiszerelési formájukat tekintve is különbözőek lehetnek, van amelyiket infúzióban adják be, de van olyan is, amelyiket szájon át alkalmaznak (kapszula/tabletta formájában). Ezen kezelések alkalmazása szigorú feltételekhez és gyakori ellenőrzésekhez kötött. Az onkoteam ítéli meg, hogy kinél alkalmazhatóak ezek a kezelések, és a beteg a kezelő orvossal közösen nyújtja be az engedélyeket az illetékes hatóságnak/hatóságoknak (NEAK, OGYÉI).
I. Érképződés gátló
VEGF-gátló
A rákos sejt a működéséhez szükséges tápanyagokat kezdetben a környezetéből veszi fel. A tumor növekedése során a tumort alkotó rákos sejtek egy idő után már nem lesznek képesek elegendő tápanyagot felvenni a környezetükből. Ekkor olyan jeleket kezdenek kibocsátani magukból, amik arra késztetik a szervezetet, hogy ereket növesszen a tumor köré és ezeken keresztül táplálja azt. Az egyik ilyen anyag, amit jelként bocsát ki a tumor a VEGF (vaszkuláris endotheliális növekedési faktor). A VEGF az egészséges szervezetben is jelen van, ez segít szabályozni az erek növekedését fejlődésünk során. A daganat esetében kórosan sok VEGF szabadul fel, és a tumor körül szabálytalan, kusza érhálózat alakul ki. Ez felborítja a tumor sejtek körüli ozmotikus nyomásviszonyokat is. Emiatt a gyógyszermolekulák is nehezebben tudnak kilépni a tumor körüli erekből és kifejteni hatásukat a rákos sejtekre.
Vannak olyan biológiai terápiák, melyeknek célja, hogy a szervezetben keringő VEGF-molekulákat megkössék. Ezzel megszüntetik a jelet, amit a tumor bocsát ki magából. Ennek hatására a tumort behálózó erek növekedése megszűnik, a már kialakult erek visszafejlődnek, rendezetté válnak, így a tumor tápanyagellátása megszűnik, a tumorsejtek nem osztódnak tovább, tápanyag híján elpusztulnak, helyreáll a tumor körüli ozmotikus nyomás is. Ezek után már más rák elleni gyógyszerek is könnyebben elérik a rákos sejteket és hatékonyabban tudják kifejteni a hatásukat a tumorra.
A VEGF-gátlók biológiai terápiák, fehérje természetű gyógyszerek. Használatukhoz nincs szükség genetikai vizsgálatokra. BRCA-mutációtól függetlenül alkalmazhatóak, többféle daganattípusban használhatóak, például vastagbéldaganat, nem kissejtes tüdődaganat, emlődaganat, hám eredetű petefészekdaganat, méhnyakrák.
Hatékonyabb a terápia, ha biztosítjuk az érújdonképződés gátlását (azaz gátoljuk a tumor körüli erek növekedését), és eközben más tumor elleni terápiával (kemoterápia, célzott terápiák) igyekszünk megakadályozni a tumorsejtek osztódását, ill. elpusztítjuk azokat. Ezért általában ezeket a terápiákat a nagyobb siker érdekében kombinálva használják.
Ezek a gyógyszerek Magyarországon is elérhetőek, sajnos nem a legolcsóbb terápiák közé tartoznak jelenleg. A finanszírozásukat a NEAK egyedi méltányosság keretein belül biztosítja, az egyedi méltányosságra vonatkozó kérelmet az onkológus indíthatja el, az onkoteam javaslata alapján. A kérelem benyújtása után 60 nap áll rendelkezésére a benyújtott kérelmek elbírálására. Pozitív válasz esetén kezdődhet el a terápia.
A VEGF-gátló gyógyszer egy oldat, amit infúzióban hígítva adnak be intravénásan, két- vagy háromhetente az onkológiai kúraszerű ellátás keretében. Az infúzió önmagában vagy más kemoterápiás szerekkel együtt adva is alkalmazható, a kezelés időtartamát protokollok szabályozzák.
A VEGF-gátló gyógyszernek lehetnek mellékhatásai, okozhat magas vérnyomást, elősegítheti sipolyok kialakulását a bélrendszerben, vagy a hüvely és a bél között, megváltoztathatja a véralvadási rendszer működését, így vérrögképződésre hajlamosíthat. A kezelőorvosodat minden furcsa tünetről tájékoztatnod kell, bármilyen onkológiai kezelésben is van részed!
Az engedélyezési „csomagot” az onkológusod állítja össze, és Neked is alá kell írni. Az engedélyt 3 majd 6 hónapos ciklusokra adják meg. A gyógyszerár-támogatási kérelmen mindig szerepeljen a telefonszámod és az e-mail címed. A kérelemről a NEAK ügyfélszolgálat telefonon ad tájékoztatást (kedd és csütörtök 9-15 óra között, a 06-1-298-2438-as telefonszámon).
Méltányossági kérelem beadásának menete:
Amikor a kivizsgálás során a rosszindulatú daganat diagnózisát megkapja a beteg (szövettani eredmény alapján általában), akkor a kezelés menetéről onkoteam kell, hogy döntsön (onkológus, sebész/nőgyógyász, patológus, radiológus. sugárterápiás szakember van benne). Itt dől el, hogy operálható vagy sem, kell-e a tervezett műtét előtt kemoterápiát kapni, vagy sem, milyen kemoterápia legyen, terveznek-e fenntartó kezelést. Ha van műtét előtti kemoterápia, akkor is kapsz még a műtét után is (általában 3 előtte, 3 utána, de ez is mindig egyénre szabott onkoteam-döntés).
Gyógyszer-finanszírozás formái Magyarországon:
· Járóbeteg gyógyszerellátás
· Egyedi méltányosság
· Fekvőbeteg intézmény
· HBCS finanszírozása
· Extrafinanszírozása
· Különkeretes gyógyszerek (hepatitis, vérzékenység)
· Tételes gyógyszerek (a NEAK természetben biztosítja)
Egyedi méltányosság kérhető
Magyarországon forgalomba hozatali engedéllyel rendelkező, de nem támogatott, különleges táplálkozási igényt kielégítő tápszerek, gyógyszerek árához.
Magyarországon forgalomba hozatali engedéllyel NEM rendelkező, de az OGYÉI véleménye/engedélye alapján rendelhető készítmények árához (egyedi import).
Indikáción túl (off-label) rendelt gyógyszerek árához.
A MEGÁLLAPÍTOTT TÁMOGATÁS ÖSSZEGÉVEL KEVESEBB TÉRÍTÉSI DÍJAT KELL A BETEGNEK FIZETNI, és utólag a támogatás összegét a forgalmazó/gyógyszertár és a NEAK elszámolja.
Egyedi méltányosság – dokumentáció
A kérelmet a kezelőorvos adja be
Célszerű az írásbeli kérelemhez már a benyújtásával egyidejűleg csatolni valamennyi kötelező mellékletet, és megadni a megfelelő adatokat, mert azok nélkül nem lehet a kérelmet elbírálni.
A kérelmet írásban a meghatározott mellékletekkel együtt kell benyújtani a NEAK-nak címezve (Nemzeti Egészségbiztosítási Alapkezelő Ártámogatási Főosztály 1139 Budapest, Váci út 73/A., Postafiók: 1565 Budapest).
A kérelem elektronikus kapcsolattartás keretében (a magyarorszag.hu kormányzati portál ügyfélkapu funkciójának kialakításáig) a meltanyossag [at] neak.gov.hu email címen nyújtható be. A kérelem elektronikus benyújtása esetén is csatolni kell valamennyi szükséges mellékletet.
- Betegkérelem-beteg aláírásával
- a beteg neve, lakcíme és TAJ száma;
- gyógyszer kiadására a beteg által megjelölt gyógyszertár megnevezése (célszerű ilyen támogatású gyógyszerek forgalmazásában gyakorlott patikát választani);
- az igényelt gyógyszerkészítmény neve;
- tartalmazhatja a beteg elérhetőségét (telefonszám, e-mail cím).
- Szakorvosi igénylőlap
- beteg személyes adatai, TAJ száma;
- igényelt gyógyszer neve, hatáserőssége, kiszerelése;
- igényelt gyógyszer dózisa (szükség esetén testsúly ill. testfelület megjelölése);
- támogatás időtartama;
- diagnózis (BNO kód);
- igénylő orvos neve, orvosi pecsétszáma, szakvizsgájának megnevezése, elérhetősége (munkahelyének megnevezése, címe, telefonszáma, esetleg e-mail címe).
- Kórtörténeti összefoglaló
- melyben a szakorvos igazolja, hogy a biztosított kizárólag az igényelt készítménnyel kezelhető hatékonyan (3 hónapnál nem régebbi);
- ismételt méltányossági kérelem esetén az adott terápia hatására bekövetkezett állapotváltozás leírása.
- Leletek másolata
- a diagnózis ill. a kérelem szerinti terápia vagy terápiaváltás szükségessége igazolása céljából (a beteg aktuális státuszának igazolásán túl a támogatás hosszabbítása esetén az összehasonlítást is segíti);
- ismételt méltányossági kérelem esetén csak a megelőző kérelem benyújtása óta eltelt időszakban bekövetkezett állapot-változást dokumentáló leletek másolata szükséges.
- Vény
- a kért támogatási időszakra szóló, de vényenként 30 napi vagy 1 ciklusnyi terápiás mennyiséget tartalmazhat
- szabályszerűen (BNO!);
- egyedi jogcímen;
- ha indikáción túli, akkor „off label” megjelölés és helyettesíthetőség megtiltása!
Elbírálás:
- A kérelem beérkezését követő naptól számított 60 napon belül.
- Indikáción túli gyógyszerrendelés egyszerűsített eljárási esetében 12 napon – belül.
- Életet veszélyeztető sürgős esetben soron kívül, azonban a szükséges dokumentumokat a beteg vagy képviselője utólag köteles csatolni.
- A megállapított méltányossági ártámogatás korlátozott időtartamra, első alkalommal legfeljebb egy évre állapítható meg.
II. PARP-gátlók

A PARP-gátlók célzott molekuláris onkológiai gyógyszerek. Ez azt jelenti, hogy nem általánosan hatnak minden osztódó sejtre, mint a kemoterápiás szerek (hiszen ezek ugyanúgy hatnak a daganatos és a nem daganatos sejtekre is), hanem célzottan csak a daganatsejtekre.
A PARP jelentése: poli ADP-ribóz polimeráz, de ezzel az elnevezésével nem igen fogsz találkozni.
A PARP-enzimek olyan fehérjék, amelyek segítenek a sejtosztódás során létrejött DNS-törések (károsodások) kijavításában. A PARP-gátlókat olyan daganatok kezelésében vezették be először, ahol egyébként is már genetikailag létezett egy hiba a javító mechanizmusban (BRCA-mutációk).
Ha hiba van a javító mechanizmusban, akkor az a jó, ha a sejt elhal. De a sejt nem tud elhalni, ha mégis “javítgatják”.
A BRCA 1 és BRCA 2 gének hasonló funkciójú javító fehérjéket kódolnak, mint a PARP, és azok az emberek, akiknél BRCA-mutáció áll fenn, hajlamosabbak bizonyos daganatfajták kialakulására, ezek az emlőrák, petefészekrák, petevezető vagy primer hashártya eredetű rákok (a továbbiakban összesítve petefészekrákokként hivatkozva), prosztatarák, hasnyálmirigyrák. A daganatsejtek, melyekben DNS-mutáció van eleve nehezebben képesek a sejtosztódás során kialakuló hibákat kijavítani, és, ha a PARP-enzimeket is blokkolják, a DNS feltöredezik, és a daganatos sejt elpusztul.
BRCA 1 és 2 mutáció lehet veleszületett vagy szerzett, utóbbi csak a tumorban van jelen.
A veleszületett BRCA-mutáció öröklődhet, ezt vérvétellel kimutatható, a vizsgálatot molekuláris genetikai laboratóriumokban végzik, az onkológus javaslatára.
A szerzett mutáció, amely a tumorszövetben alakul ki a későbbiekben, a műtét során vett szövetmintából mutatható ki, ezt az onkológiai centrumok patológiai laboratóriumaiban tudják kimutatni.
Mindkét vizsgálat az egészségbiztosítás keretében ingyenes - bár van magánfinanszírozott formában is -, ami a későbbi kezelés meghatározása miatt jelentős információ. Amennyiben a családban előfordult bármilyen ágon emlő- vagy petefészekrák, aránylag fiatal korban, mindenképpen érdemes elvégeztetni ezt a vizsgálatot, sőt, a gyermekeidre is gondolj, hiszen ők is örökölhetik. Az egyenesági hozzátartozók és a testvérek szűrését is a molekuláris genetikai laboratóriumok OEP-finanszírozás keretében elvégzik.
Ezen biológiai kezelések szigorú feltételekhez kötöttek (alább részletezzük), és a kezeléshez az engedély egyedi méltányossági kérelem benyújtását követően kapható meg. Ezeket az adminisztratív lépéseket (a mintából végzett tumorgenetikai vizsgálat, az egyedi méltányossági kérelem összeállítása) a kezelőorvos végzi el, az alábbi tájékoztató segítség lehet abban, hogy mely esetekben jön szóba az ilyen irányú kezelés.
Amennyiben úgy érzed, hogy az alábbi kezelések valamelyike szóba jöhet az esetedben, akkor fordulj bizalommal valamelyik, a Mályvavirág Alapítvánnyal kapcsolatban álló petefészekrák-centrumhoz. Fontos tudnod, hogy Magyarországon az OEP finanszírozott ellátás keretében mindenkinek joga van másodvéleményt kérni, másik szakembert felkeresni. Ha úgy érzed, nem vagy elégedett, nem vagy biztos benne, hogy minden lehetőséget ismertettek Veled, vagy csak egyszerűen nem szimpatikus a kezelőorvosod, segítünk másik szakembert találni. Az orvos-beteg kapcsolat bizalmi kapcsolat, ami nem csak professzionális szinten befolyásolja a gyógyulásodat.
Amennyiben grade 2-3 (magas malignitású, szövettanilag differenciálatlan) hám eredetű petefészekrákod van, a kezelése folyamán több ponton is szóba jön a PARP-gátlókkal történő kezelés.
A törvény szerint minden onkológiai betegséggel kapcsolatos döntés onkológiai bizottsági (ún. onkoteam = onkológus szakorvos, daganatsebész szakorvos, patológus szakorvos) véleményezés után történhet, így ez értelemszerűen vonatkozik a fenntartó kezelésekre is.
1. Kiújult hám eredetű petefészekrák esetén adható a PARP-gátló fenntartó kezelés, ha az ismételt platina alapú kemoterápiára legalább részleges tumorválasz következett be, BRCA 1 / 2 mutáció jelenlétében.
2. A PARP-gátló kezeléseket önmagában adják fenntartó kezelésként.
3. Kiújult esetekben a BRCA 1 / 2 mutáció hiányában is szóba jön a PARP-gátlóval végzett fenntartó kezelés, azonban ezekben az esetekben a hatásosság elmarad a BRCA-mutáció esetében tapasztalttól.
Amennyiben szóba jönnek a PARP-gátlókkal végzett fenntartó kezelések, úgy a kemoterápiás kezelés (rendszerint 6 ciklus) legkésőbb 4. ciklusáig a kivett daganatból tumorgenetikai vizsgálatot kell kérjen a kezelőorvos, mert a vizsgálat és az engedélyezés időigényes folyamata miatt így biztosítható, hogy a kemoterápiás kezelés után a szükséges 8 héten belül megkapd a kezelést és ne csússz ki az időablakból.
Az engedélyezési „csomagot” az onkológusod állítja össze, és Neked is alá kell írni. Az engedélyt 3 majd 6 hónapos ciklusokra adják meg. A gyógyszerár-támogatási kérelmen mindig szerepeljen a telefonszámod és az e-mail címed. A kérelemről a NEAK ügyfélszolgálat telefonon ad tájékoztatást (kedd és csütörtök 9-15 óra között, a 06-1-298-2438-as telefonszámon).
A PARP-gátlókkal végzett kezelés elindításának is vannak ellenjavallatai, erről kezelőorvos tájékoztat, pl. ha a megelőző kemoterápiás kezelési sorozat nehezen uralható csontvelő-elégtelenséget okozott.
A PARP-gátlókkal végzett fenntartó kezelések általában jól tolerálhatóak, a leggyakoribb előforduló mellékhatások a csontvelő visszafogott működésére vezethetők vissza (elsősorban vérszegénység, illetve a fehérvérsejtszám csökkenése), mely fertőzésekre hajlamosíthat, illetve a betegek egy részénél emésztési panaszok, hányinger, hasmenés, fáradtság, étvágytalanság jelentkezhetnek. Mellékhatások észlelése esetén konzultálj a kezelőorvossal a teendőkről!
Fontos kényelmi szempont, hogy a kezelés szájon át történik, és nem szükséges infúziós kezelésekre a kórházba járni. A kezelés alatt rendszeres vérkép vizsgálatot fognak végezni (az első évben havonta) a mellékhatások észlelésére. Szükség esetén a kezelőorvos az előírt gyógyszer mennyiségének csökkentését írhatja elő. A kezelés folyamatosan adható amíg a tumort gátolja, ennek igazolására állapotodat háromhavonta CT vizsgálatokkal ellenőrzik. Azon betegek esetében ahol a kezdeti CA125 tumormarker érték emelkedett volt ennek ellenőrzését is felhasználják az utánkövetésben.
A PARP-gátlókkal végzett fenntartó kezelés időtartama általában 2 év, de hosszabb ideig is alkalmazható. Jelenleg is folynak kutatások, klinikai vizsgálatok, amelyekben PARP-gátlókat vizsgálnak önmagukban vagy más gyógyszerekkel együtt adva.
A PARP-gátló kezelések nem csak a betegségmentes túlélés növekedésében hatékonyak, de bizonyítottan és jelentősen növelik a betegek teljes túlélését is.
Méltányossági kérelem beadásának menete:
Amikor a rosszindulatú daganat kiújul, akkor a kezelés menetéről onkoteam kell, hogy döntsön (onkológus, sebész/nőgyógyász, patológus, radiológus van benne). Itt dől el, hogy operálható vagy sem, kell-e a tervezett műtét előtt kemoterápiát kapni, vagy sem, milyen kemoterápia legyen, terveznek-e fenntartó kezelést. Ha van műtét előtti kemoterápia, akkor is kapsz még a műtét után is (általában 3 előtte, 3 utána, de ez is mindig egyénre szabott onkoteam döntés). Ideálisan legkésőbb az első onkoteamen döntenek arról is, hogy végezzenek-e BRCA-vizsgálatot és ezt el is indítják (kb. 1 hónapon belül van eredmény). Az Egyedi Méltányossági Kérelem beadására akkor kerülhet sor, ha pozitív a BRCA-lelet, és a beteg megkapott kb. 4 platinabázisú kezelést (ez attól is függ, hogy hány kezelést terveznek), és a kontroll CT, tumormarker is rendben van. Lehet, hogy míg a kérelmed a NEAK jóváhagyásra vár, még kapsz további kezeléseket. Ha megjön az engedély, leghamarabb az utolsó kezelés után 3 héttel kezdhető el a fenntartó PARP-kezelés, ha a vérképed rendeződött, de erre van egyébként 8 hét (3-8 hét között kell elkezdeni a kezelést).
Gyógyszerfinanszírozás formái Magyarországon:
- Járóbeteg gyógyszerellátás
- Egyedi méltányosság
- Fekvőbeteg intézmény
- HBCS finanszírozása
- Extrafinanszírozása
- Különkeretes gyógyszerek (hepatitis, vérzékenység)
- Tételes gyógyszerek (a NEAK természetben biztosítja)
Egyedi méltányosság kérhető
- Magyarországon forgalomba hozatali engedéllyel rendelkező, de nem támogatott, különleges táplálkozási igényt kielégítő tápszerek, gyógyszerek árához
- Magyarországon forgalomba hozatali engedéllyel NEM rendelkező, de az OGYÉI véleménye/engedélye alapján rendelhető készítmények árához (egyedi import)
- Indikáción túl (off-label) rendelt gyógyszerek árához
A MEGÁLLAPÍTOTT TÁMOGATÁS ÖSSZEGÉVEL KEVESEBB TÉRÍTÉSI DÍJAT KELL A BETEGNEK FIZETNI, és utólag a támogatás összegét a forgalmazó/gyógyszertár és a NEAK elszámolja.
Egyedi méltányosság – dokumentáció
A kérelmet a kezelőorvos adja be
Célszerű az írásbeli kérelemhez már a benyújtásával egyidejűleg csatolni valamennyi kötelező mellékletet és megadni a megfelelő adatokat, mert azok nélkül nem lehet a kérelmet elbírálni.
A kérelmet írásban a meghatározott mellékletekkel együtt kell benyújtani a NEAK-nak címezve (Nemzeti Egészségbiztosítási Alapkezelő Ártámogatási Főosztály 1139 Budapest, Váci út 73/A., Postafiók: 1565 Budapest).
A kérelem elektronikus kapcsolattartás keretében (a magyarorszag.hu kormányzati portál ügyfélkapu funkciójának kialakításáig) a meltanyossag [at] neak.gov.hu email címen nyújtható be. A kérelem elektronikus benyújtása esetén is csatolni kell valamennyi szükséges mellékletet.
• Betegkérelem-beteg aláírásával
• a beteg neve, lakcíme és TAJ száma;
• gyógyszer kiadására a beteg által megjelölt gyógyszertár megnevezése (célszerű ilyen támogatású gyógyszerek forgalmazásában gyakorlott patikát választani);
• az igényelt gyógyszerkészítmény neve;
• tartalmazhatja a beteg elérhetőségét (telefonszám, e-mail cím).
• Szakorvosi igénylőlap
• beteg személyes adatai, TAJ száma;
• igényelt gyógyszer neve, hatáserőssége, kiszerelése;
• igényelt gyógyszer dózisa (szükség esetén testsúly ill. testfelület megjelölése);
• támogatás időtartama;
• diagnózis (BNO kód);
• igénylő orvos neve, orvosi pecsétszáma, szakvizsgájának megnevezése, elérhetősége (munkahelyének megnevezése, címe, telefonszáma, esetleg e-mail címe).
• Kórtörténeti összefoglaló
• melyben a szakorvos igazolja, hogy a biztosított kizárólag az igényelt készítménnyel kezelhető hatékonyan (3 hónapnál nem régebbi);
• ismételt méltányossági kérelem esetén az adott terápia hatására bekövetkezett állapotváltozás leírása.
• Leletek másolata
• a diagnózis ill. a kérelem szerinti terápia vagy terápiaváltás szükségessége igazolása céljából (a beteg aktuális státuszának igazolásán túl a támogatás hosszabbítása esetén az összehasonlítást is segíti);
• ismételt méltányossági kérelem esetén csak a megelőző kérelem benyújtása óta eltelt időszakban bekövetkezett állapot-változást dokumentáló leletek másolata szükséges.
• Vény
• a kért támogatási időszakra szóló, de vényenként 30 napi vagy 1 ciklusnyi terápiás mennyiséget tartalmazhat;
• szabályszerűen (BNO!);
• egyedi jogcímen;
• ha indikáción túli, akkor „off label” megjelölés és helyettesíthetőség megtiltása!
Elbírálás:
- A kérelem beérkezését követő naptól számított 60 napon belül.
- Indikáción túli gyógyszerrendelés egyszerűsített eljárási esetében 12 napon – belül.
- Életet veszélyeztető sürgős esetben soron kívül, azonban a szükséges dokumentumokat a beteg vagy képviselője utólag köteles csatolni.
- A megállapított méltányossági ártámogatás korlátozott időtartamra, első alkalommal legfeljebb egy évre állapítható meg.
HORMONTERÁPIA
A hormonterápia egy olyan kezelési mód, amelynek hatására a szervezet leállítja bizonyos hormonok termelését, vagy a hormonok hatását.
A hormonok kémiai hírvivők, amiket a belső elválasztású mirigyek, mint például a petefészek, here, hasnyálmirigy, pajzsmirigy termelnek, és amelyek a szervezet működését szabályozzák.
A hormonterápia nem elsődleges kezelési módszer petefészekrák esetén, de például kiújulás esetén egyéb terápiák kiegészítéseként alkalmazható. Az ösztrogén és a progeszteron elősegítheti a petefészekrák fejlődését. Az ösztrogént legnagyobb részben a petefészkek termelik, kisebb részben a máj és a mellékvesék. A progeszteront szintén leginkább a petefészkek termelik. Ezen hormonok termelésének leállítása vagy a hormonszint csökkenése elősegítheti a petefészekrák fejlődésének lassulását.
A hormonterápia is számos enyhe vagy komoly mellékhatást okozhat. Előfordulhatnak menopauzás tünetek, mint a hőhullám, hangulatváltozás, hüvelyszárazság, nyugtalan alvás, éjszakai izzadás. Jelentkezhet hüvelyi váladékozás, súlynövekedés, a végtagok megdagadása, fáradtság, csökkent szexuális vágy. Ezek csak az általánosan előforduló mellékhatások, ezek mellett jelentkezhetnek más tünetek is, melyekről konzultálni kell az orvossal.
Petefészekdaganatok esetében külön kérésre végzik a hormonvizsgálatot, rutinszerűen nem.
Terápiahűség: beteg együttműködés
Amikor egy terápia megfelelő, akkor a betegnek is van kötelezettsége. Az, hogy betartsa az orvos utasításait, javaslatait, szedje a gyógyszert az előírtaknak megfelelően, vagy, ha laborvizsgálatokhoz, kontrollokhoz kötött a terápia, akkor azokon a megfelelő időben jelenjen meg. Ezt nevezzük terápiahűségnek.
Titkos és zárt csoport a terápia témában:
https://www.facebook.com/groups/360804698536521/member-requests
Klinikai vizsgálat

Az orvostudományban egyre nagyobb szerep jut a klinikai vizsgálatoknak. A tudomány és a technika fejlődése lehetőséget teremt számos gyógyszer és orvostechnikai eszköz kifejlesztésére, de sajnos vannak még olyan betegségek, amelyek terápiája megoldatlan. A klinikai kutatások célja, hogy új terápiás lehetőségeket teremtsenek, vagy már ismert gyógyszer indikációját bővítsék.
A klinikai vizsgálat nem emberkísérlet! Egy hatóanyag az embereken történő kipróbálásáig hosszú úton megy keresztül, mint pl. a laboratóriumi vizsgálatok, állatkísérletek. Csak olyan hatóanyagok kerülnek emberi alkalmazásra, melyek biztonságossága és hatékonysága előzetes vizsgálatok során igazolódott.
A klinikai vizsgálatokat szigorú etikai, törvényi és szakmai szabályozás (Helsinki nyilatkozat, GCP, hazai rendeletek) alapján végzik. Bizonyíték kell, hogy a hatóanyag hatásos és nem ártalmas.
Klinikai vizsgálatok humán fázisai:
I. fázis: Első alkalommal próbálják ki emberen az új hatóanyagot. Egészséges önkéntesek vesznek részt / kivéve onkológiai készítmények esetén. Hatóanyag-eloszlás vizsgálata, dózis meghatározása, felszívódás és kiürülés vizsgálata történik ebben a szakaszban. Mellékhatások, biztonságosság.
II. fázis: Arra szolgál, hogy eldöntsék, a hatóanyag alkalmas-e gyógyításra. Kis létszámú csoporton végzik a vizsgálatot. Biztonság, tolerálhatóság, terápiás hatás, optimális adag meghatározása történik ebben a fázisban.
III. fázis: A II. fázis megerősítése nagyszámú beteganyagon, így a legtöbb beteg ebbe a fázisba kapcsolódik be. Biztonságosság, hatásosság, mellékhatások, más készítményekkel való összehasonlítás történik ebben a lépésben. 2 évig figyelni kell a készítményt a bevezetést követően.
IV. fázis: a forgalomba került készítményt vizsgálja, hosszú távú hatásosságát és biztonságosságát, költséghatékonyságát és ritka mellékhatásait.
A klinikai vizsgálatokat magáncégek/gyógyszercégek szponzorálják. Hitelességre törekednek, így minden vizsgálóhelyen ugyanazon feltételeknek kell teljesülniük. Minden szigorúan szabályozott. A vizsgálati helyek protokollok alapján dolgoznak. A vizsgálatok hosszú évekig tartanak, és rengeteg költséggel járnak. Ha nem válik be, akár csődbe is mehet a gyógyszercég.
Ki vehet részt egy klinikai vizsgálatban?
Olyan cselekvőképes személyek, akik előzetesen megfelelő tájékoztatást kaptak, megértették a vizsgálatról kapott információkat, és önként, befolyásolásmentesen, szabadon döntöttek a részvételről. A résztvevők bármikor, indoklás nélkül kiléphetnek a vizsgálatból, amelyekbe korábban beleegyeztek. Személyes adatok semmilyen módon nem kerülnek nyilvánosságra. Szigorú bevonási és kizárási kritériumoknak kell megfelelnie a bevont személynek. Beteg bevonásakor döntő tényező a kórelőzmény, az aktuális állapota és laboratóriumi paraméterei. A beteg nem kérheti (én akarom), és a háziorvos sem javasolhatja (hiszen nem mindenhol elérhető).
Ha a szponzor által a teljes statisztikai értékelése megtörtént a kutatásnak, és közölte az eredményeket a vizsgáló orvossal, személyes tájékoztatást kaphat a vizsgálatban résztvevő. Klinikai vizsgálatok eredményeit tudományos előadásokon és orvosi szakirodalomban is megjelentetik.
A klinikai vizsgálattal a beteg új, akár sikeresebb kezelési lehetőséget kaphat. A szponzor piacot nyer.
Az innováció erőforrás- és költségigényes, egy gyógyszer kifejlesztése kb. 10.000 vegyületből kezdődik, alig néhány 100 jut el laboratóriumi vizsgálatig, még kevesebb az állatkísérletig, és pár hatóanyag jut el a humán fázisig. 12 év: 4 év preklinikai és 8 év humán vizsgálat. A gyógyszerjelölt a forgalomba hozatali engedély birtokában gyógyszerként kerülhet forgalomba.
Placebo – hogy valósul meg az onkológiai vizsgálatokban?
Onkológiában nincs placebo! Hátrány nem érheti a beteget!
Olyan kórképekben lehetséges, amelyben hatóanyag nélküli kezelés alatt a betegség nagyfokú romlását nem eredményezi. Az onkológiai klinikai vizsgálatokban a betegek a vizsgálati karon, a vizsgálni kívánt hatóanyagot kapják meg, önmagában vagy a korábbi hagyományos terápiákkal kiegészítve, a kontroll karon pedig általában a korábbi hagyományos kezelést. A vizsgálatban ennek a két terápiás lehetőségnek az eredményességét hasonlítják össze. Egyes esetekben előre meghatározott kritériumok alapján, amennyiben a vizsgált hatóanyaggal kiemelkedő eredményt igazoltak, a kontroll karon lévő betegek a daganat rosszabbodását/kiújulását követően megkaphatják a vizsgálati készítményt. Ezt a lehetőséget nevezzük “cross overnek”.
Vizsgálat típusai:
Nyílt vizsgálat: nyilvános a hatóanyag. A beteg és az orvos is tudja, hogy a beteg a vizsgálati vagy a kontroll karon van-e.
Vak vizsgálat: a beteg vagy a beteg és az orvos számára is titkolt a hatóanyag. Sem a beteg, sem az orvos nem tudja, hogy a vizsgálati vagy a kontroll karra került-e a beteg. A vizsgálat lezárásakor egyes esetekben nyitottá teszik a vizsgálatot.
Egykarú: aki bekerül a vizsgálatba, kapja a vizsgált hatóanyagot.
Több karú: több hatóanyag, vagy hatóanyag és placebo alkalmazása.
Cross over: ha a vizsgálat egyik karja olyan sikereket ér el, hogy más karokból is átdelegálják a betegeket.
A klinikai vizsgálatokhoz tartozik:
IMMUNTERÁPIA - még klinikai vizsgálatok alatt van petefészekrák betegségre
Immunrendszerünk nem csak a kívülről jött kórokozókkal szemben lép fel hatékonyan, de a szervezeten belül keletkező elfajult sejteket is igyekszik elpusztítani. A daganatok túlélésének egyik legfontosabb feltétele az immunrendszer elöli „elbújás”. Minden daganat, mely nagyobb méretet ér el vagy már áttétet is képzett, sikeresen bújt el az immunrendszer elől, különböző technikákkal, „maszkírozta magát”. A daganatok elpusztításának hatékony módszere, ha a szervezet saját immunrendszerének segítünk a daganat felismerésében. Erre szolgálnak az ún. immunterápiák.
Az ún. „checkpoint-gátlók” csoportjába tartozó szerek az immunrendszer T-sejtjein található PD1 receptor gátlásával teszi lehetővé, hogy az immunsejtek visszanyerjék a daganatos sejteket pusztító képességüket.
Ez a kezelés akkor jön szóba, ha a beteg előrehaladott hámeredetű petefészekrákban szenved, és a daganatából jelentős ún. mikroszatellita instabilitás (MSI-H) vagy a „mismatch” javító mechanizmus zavara (dMMR) igazolható. Ebben az esetben várható, hogy a fenti kezelés hatékonyan serkenti az immunrendszerét a daganattal szemben. A daganat fenti jellemzőit a korábban eltávolított tumorblokkból utólag határozzák meg, ehhez sem szükséges újabb mintavétel. Ez a kezelés a standard kemoterápiás kezelések (fenntartó kezelésekkel vagy anélkül) sikertelensége esetén jön szóba.
Onkológusodtól érdeklődj a klinikai vizsgálat lehetőségéről.
A linkek eléréséhez kattints a címekre!
Nőgyógyászati Daganatsebészeti Centrum
Klinikai vizsgálatok oldal:
Rehabilitáció
A rehabilitáció a diagnózis felállításától kezdődik. Sok esetben azt gondoljuk, hogy a rehabilitáció nem releváns, de a rehabilitáció sokkal tágabb fogalom, mint hinnénk. Átkarolja az életminőség megtartását, fejlesztését. Sokkal nagyobb perspektívában kell gondolnunk rá, mert segítséget, támogatást ad már a betegút elejétől is. Kísér, felkészít, segít, lehetőségeket biztosít, regenerál, összeköt.
A rehabilitációt, a Mályvavirág Alapítványnál Gyógyulást Segítő Programnak hívjuk. Röviden GYSP-nek nevezzük, amely több elemet foglal magába.
Fizikai/testi rehabilitációról és lelki rehabilitációról beszélhetünk.
A lélek útja
A diagnózis-sokktól, a kezeléseken való részvételeken át, a nőiesség megélésén, a félelmeken, a reményen és reményvesztésen, a hullámhegyeken és hullámvölgyeken keresztül, a kiújulástól való félelemig, vegyesen és egyénileg éljük meg a betegséget. Ráadásul a betegségben nem egyedül vagyunk, ott van a család, barátok, a környezet, amihez tartozunk.
A félelemnek is több arca van, állandó lakóvá válik az életünknek, bár ez is egyéni, van, akinél erősebben, van, akinél kevésbé jelentkezik.
Fel kell dolgoznunk, ami velünk történik, és olykor egy mókuskerékbe csöppenünk, ahol a lelki generálja a fizikai gátat és a fizikai a lelkit. Ilyenkor meg kell akasztani ezt a kereket, s ehhez van, hogy segítségre van szükségünk.
Egy pszichológus szakember segítsége, vagy valamilyen alternatív, kiegészítő segítség jól jöhet. Rengeteg ilyennel találkozhatunk, és mindenkinek meg kell találnia azt, amiben hinni tud, mert a hit mindig erősít és utat mutat.
Dolgozunk pszichológusokkal is, akiket megtalálsz itt:
https://malyvavirag.hu/szakmai-bizottsag
A linkek eléréséhez kattints a címekre!
A Mályvavirág Alapítvány szexuális egészséggel foglalkozó weboldala
A lélek segítésére készítettük el foglalkoztató kiadványunkat:
Lelkemnek - Igényeld meg tőlünk a nyomtatott példányt: info [at] malyvavirag.hu
Mályvaspájz - dietetikai könyv
A libidó elvesztése a rák után
Menopauza a nőgyógyászati daganatok után
A segítő segítője - Hozzátartozók kiadványa
Fizikai rehabilitációt segítő kiadvány:
Palliatív ellátás
A palliatív ellátás a terminális állapotú betegek tüneteinek enyhítésére irányuló támogató kezelések összessége. Az egészségügyi világszervezet (WHO) 2002-ben a következőképpen fogalmazta meg a palliatív ellátást:
„A palliatív ellátás olyan megközelítés, amely az életet megrövidítő betegség kísérő problémáitól szenvedő páciens és családja életminőségét javítja azáltal, hogy megelőzi és csillapítja a szenvedést a fájdalom, a fizikai, pszichoszociális és spirituális problémák meghatározásával, kifogástalan értékelésével és kezelésével.”
A palliatív gondozás céljai:
- csillapítja a fájdalmat és az egyéb kínzó tüneteket;
- az életet és a halált normális folyamatnak tartja;
- nem tesz semmit a halál megrövidítése és meghosszabbítása érdekében;
- integrálja a betegellátásba a pszichológiai és spirituális tényezőket;
- támogató rendszert kínál, hogy a beteg a lehető legaktívabban élhessen a halálig;
- támogató rendszert kínál a család számára a betegség ideje alatt és a gyász időszakában;
- team-munkát alkalmaz, amely a beteg és családja szükségleteire irányul, beleértve a gyász-tanácsadást, ha az javasolt;
- kiemeli az életminőséget, ugyanakkor pozitívan viszonyul a betegség folyamatához;
- alkalmazható a betegség korai stádiumában, az életet meghosszabbító terápiákkal – mint a kemoterápia és radioterápia – együtt, és magában foglalja azokat a szükséges vizsgálatokat is, amelyek szükségesek a kínzó klinikai komplikációk jobb megértéséhez és kezeléséhez.
A palliatív gondozás során az orvos a beteggel való megállapodás alapján lemond az aktív gyógykezelésről, mivel meggyógyítására az orvostudomány aktuális fejlettségi szintjén nincs remény, de célja nem a beteg halálának előidézése, hanem a beteg utolsó heteinek, hónapjainak emberibbé tétele, életminőségének javítása.
A megfelelő időben elkezdett palliatív ellátás során nem csak életet adhatunk a napoknak, hanem napokat is adunk az életnek, hiszen a korán megkezdett palliatív ellátás során egy olyan multidiszciplináris csoport foglalkozik a betegekkel, amely a betegek állapotához és igényeihez igazodó ellátást képes nyújtani.
Fájdalomcsillapítás a palliatív ellátásban
Mi is a fájdalom?
“Olyan kellemetlen szenzoros és emocionális élmény, amelyet a szövetek aktuális vagy potenciális károsodása okozza.”
Tehát a fájdalom egy teljesen szubjektív érzet, mely függ a beteg általános fizikai, lelki, szociális és mentális állapotától. A rák diagnózisának megállapításakor a betegek egynegyede, a kezelések során pedig az egyharmada, míg a daganatos betegség előrehaladottabb állapotában a betegek háromnegyede panaszol jelentős fájdalmat. A fájdalom mértékének megállapításában segítség lehet a fájdalommérő skála (numerikus skála, verbális skála stb.), hiszen, habár a fájdalom szubjektív, az erős, intenzív, súlyos fájdalmaknak vannak testi tünetei mint például a mimika, a mozgás és a testtartás.
Rettentően fontos a fájdalom megfelelő csillapítása mind a kezelések során, mind a palliatív ellátás alatt. A csillapíthatatlan erős fájdalom kihatással van a beteg teljes életére, emberi kapcsolataira, befolyásolhatja a táplálkozását, alvását, fokozza a szorongást, depresszióhoz vezethet, és megnehezíti a betegséggel való megküzdést.
A daganatos betegségekben a fájdalom az esetek 80%-ában viszonylag jól csökkenthető, mégis a betegek jelentős hányada szenved átmeneti vagy tartós fájdalomtól. Ezért szükséges az egyénnek legmegfelelőbb fájdalomcsillapítási módszer kiválasztása. A sikeres fájdalom kezeléséhez kulcsfontosságú a daganatos fájdalom okainak, patomechanizmusának feltárása, a megfelelő gyógyszer megfelelő adagjának megválasztása.
Fájdalom okai sokrétűek lehetnek a daganatos betegségek esetén. A testi okok közül jelentős a daganat vagy áttétei által kiváltott kompresszió, nyomás a környező szervekre, illetve roncsolás, mely a lágyszöveti duzzanatot, a zsigeri szervek falának feszülését, másodlagos szöveti hypoxiát (szöveti oxigén elégtelenséget), az idegi struktúrák nyomását, infiltrálódását vagy a környező szervi képletekbe való beszűrődését, átszövését, a csontállomány meggyengülését eredményezi. A daganat környezetében gyakran van jelen gyulladás, mely szintén fájdalmat okoz. A fájdalom oka lehet maga a daganat elleni kezelés, akár sebészi, akár kemoterápiás, akár sugárterápiás kezelésről beszélünk.
Palliatív ellátás során figyelembe kell vennünk a fájdalom szempontjából a legyengült szervezetet, amely sok pihenést igényel, ezáltal fájdalmat okozhat a tartós fekvés következtében kialakuló izommerevség és az ízületek beszűkülése is, vagy akár a kialakuló felfekvés (decubitus).
A testi okokon túl nagy szerepet játszik a fájdalom mértékében a kialakuló szorongás, a halálfélelem, a kezeléssel kapcsolatos félelmek, a gondozásra szoruló családtagok, kiskorú gyermekek hátrahagyása miatti aggódás, az egyes panaszok elviselésének képessége mind-mind befolyásolják a kialakult fájdalom érzet intenzitását. Mindezeken túl az élet vége felé felszínre törhetnek olyan gondolatok, mint például a leélt élet értelme, lelkiismeret-furdalást okozhatnak a halogatott és meg nem tett kötelességek, vágyak vagy jelen lehet a spirituális düh a sorssal szemben.
Fájdalmat leggyakrabban gyógyszeres kezeléssel csillapítunk, de vannak esetek amelyek során oki kezelést is alkalmazhatunk, mely során a felderített fájdalom okát próbálják megszüntetni. Ezért a daganatos betegek fájdalomcsillapítása során alkalmazhatunk sebészi, radiológiai, kemoterápiás, hormonterápiás, biológiai válaszmódosító, fizioterápiás, pszichoterápiás vagy akár egymást kiegészítő kezeléseket. Komplementer terápia esetén szóba jöhet az akupunktúra, bizonyos mágnesterápiás eljárások, aromaterápia, zeneterápia, művészetterápia, amelyek mind a fájdalomcsillapítás multimodális kiegészítő részei.
Gyógyszeres fájdalomcsillapítás esetén is széles skálából választhatjuk ki a fájdalom típusának, intenzitásának és mértékének megfelelően. Fontos, hogy a fájdalomcsillapító terápia során megfelelően szakképzett orvosok és ápolók segítsék terápiánkat, ezért ilyenkor érdemes felkeresni a fájdalom ambulanciákat.
Fájdalomcsillapító terápia során lépcsőzetes terápiát alkalmazunk, mely segít kordában tartani a fájdalmat. Háromlépcsős algoritmust alkalmazunk, amely aszerint oszlik meg, hogy a gyengén és közepesen erős fájdalomcsillapítók - melyeknek van maximum dózisa - tartoznak az első és második lépcsőfokhoz. A maximum dózis azt jelenti, hogy egy adott készítmény meghatározott mennyiségen, pl. 200 mg-on felül már nem hatásos - nem csillapítja a fájdalmunkat -, sőt, veszélyes is a maximális dózis felett alkalmazni. Ezt követően a harmadik lépcsőfokhoz olyan típusú gyógyszerek tartoznak, amelyek már erős ópiátok és nincsen maximális dózisuk, így bizonyos szabályok betartása mellett - ha szükséges -, fokozatosan magas tartományba emelhetők.
A fájdalomcsillapítókat lépcsőzetesen vezetjük be, enyhébb fájdalmak esetén egyszerű analgetikumokat, NSAID-okat (nem-szteroid gyulladáscsökkentőket) alkalmazunk, ha pedig elégtelenné váltak, abban az esetben gyenge majd erős ópiumokkal egészítjük ki azokat. Fontos betartani a fájdalomcsillapítás során a lépcsőzetes emelést, hiszen vannak bizonyos készítmények, mint az ópiátok, melyek addikciót - vagyis hozzászokást - váltanak ki. A kialakult függőség pedig magával hozza, hogy időnként szükséges a fájdalom megfelelő csillapítása érdekében tovább emelni a dózist.
Számolni kell a fájdalomcsillapítók mellékhatásaival is, amelyek lehetnek szív- és érrendszeri következmények, székrekedés, hányinger, hányás, álmosságérzet-fokozódás, aluszékonyság (szedáció), krónikus fájdalomcsillapítás során alkalmazott ópiátok esetén akár légzésdepresszió, zavartság, mentális állapotromlás, szájszárazság, vizeletretenció (visszatartás), verejtékezés, endokrin és immunológiai változások.
Fájdalom kezelése során megkülönböztetünk speciális fájdalomformákat is, mint az áttöréses fájdalom, amely során “a beteg által megélt fájdalom átmeneti fokozódását értjük, amikor a bazális fájdalom relatíve stabil, és megfelelően kontrollált. Az áttöréses fájdalom olyan rövid periódusokat jelent, amit a rendszeresen használt ópiát-dózis nem csillapít megfelelően.” Ilyen típusú fájdalom felléphet akár hasi colica esetén.
Speciális fájdalmak közé tartozik a neuropátiás fájdalom, amely az idegrendszer károsodása, vagy működési zavara következtében kialakult fájdalom. Előrehaladott tumoros betegségekben (nyirokcsomóba szóródó méhnyakrák, áttétet adó fej-nyaki tumorok, hasnyálmirigy farok tumor, mellkasfalat érintő emlődaganat esetén) 30%-ban előforduló fájdalomtípus. Viszonylag ritka fájdalomtípus a tenesmoid hólyag és végbél fájdalom, de okozhatja hólyagtumor, vagy nemi szervi tumor, mely átterjed a hólyagra és végbélre. A tenesmoid (lüktető) típusú fájdalmat kínzó, fájdalmas, tolófájás szerű székelési illetve frusztrán imperatív/kényszerítő vizelési ingerek jellemzik. Ilyen típusú fájdalom jelentkezése esetén fontos kizárni a húgyúti fertőzés és a székletrög lehetőségét.
Előrehaladott daganatos betegségben jól alkalmazható fájdalomcsillapítók rendszerint vénykötelesek, amelyeket kezelőorvosunk, illetve háziorvosunk tud felírni számunkra. Daganatos betegség okozta fájdalom csökkentésre valamennyi gyenge és erős ópiátot szakorvosi javaslat nélkül, kiemelt támogatással rendelhet orvosunk. Rendszeresen erős ópiáttal való kezelés esetén kizárólag háziorvosunk jogosult a készítmény felírására. A háziorvos egy hónapra elegendő gyógyszert rendelhet, melyet mindig ugyanabban a patikában kell kiváltani. A készítmény rendszeres rendeléséről a háziorvos három havonta gyógyszertári értesítővel tájékoztatja a patikát. A fel nem használt ópiátkészítményeket pedig kötelesek vagyunk a patikába visszavinni.
A fájdalom ambulancia több orvosi szakterület képviselőinek összehangolt munkájára épül, így a fájdalommal küzdő betegeknek nem kell orvostól orvosig járniuk, hogy megoldást találjanak a problémáikra. A fájdalom ambulancia tapasztalt orvosai hatékonyan csillapítják a hosszabb ideje fennálló, krónikus fájdalmat.
Fájdalom Ambulanciák, melyek daganatok okozta fájdalom csillapítással foglalkoznak Magyarországon:
- Békéscsaba-Gyula
- Békés Megyei Pándy Kálmán Kórház: https://bmkk.eu/
- Debrecen
- Debreceni Egyetem Klinikai Központ Szülészeti és Nőgyógyászati Klinika: https://noiklinika.unideb.hu/
- Budapest
- Országos Onkológiai Központ: https://onkol.hu/betegeknek/fekvo-es-jarobeteg-ellatas/fajdalomcsillapitasi-ambulancia/
- SOTE/Semmelweis Egyetem Neurológiai Klinika: https://semmelweis.hu/klinikaikozpont/
- Uzsoki Utcai Kórház: https://www.uzsoki.hu/neurologiai-ambulancia
- Országos Idegtudományi Intézet, https://okiti.hu/jarobeteg-ellatas/fajdalomambulancia.html
- Jahn Ferenc Dél-Pesti Kórház,https://www.delpestikorhaz.hu/jarobeteg-ellatas/ambulanciak/fajdalom-ambulancia/
- Bajcsy-Zsilinszky Kórház, https://bajcsy.hu
- Szent Margit Kórház: https://www.szentmargitkorhaz.hu/a-korhazrol/jarobeteg-ellatasszakrendelesek/fajdalomambulancia/
- Szolnok
- Hetényi Géza Kórház: http://www.hetenyikorhaz.hu/aneszteziologiai-es-intenziv-terapias-osztaly
- Kaposvár
- Somogy Megyei Kaposi Mór Oktató Kórház: http://www.kmmk.hu/betegellatas/szakrendelesek/
- Kecskemét
- Bács Kiskun Megyei Kórház Onkoradiológiai Központ: https://www.kmk.hu/kecskemet/fekvobeteg-osztalyok/339-onkoradiologiai-koezpont
- Győr
- Petz Aladár Egyetemi Oktatókórház: https://www.petz.gyor.hu/
- Miskolc
- B-A-Z Megyei Központi Kórház: https://www.bazmkorhaz.hu/
- Nyíregyháza
- Szabolcs-Szatmár-Bereg Megyei Kórházak és Egyetemi Oktatókórház: http://www.szszbmk.hu/hireink/368-nyiregyhaza-az-onkologiai-ellatas-elvonalaban
- Pécs
- Pécsi Tudományegyetem, Aneszteziológiai és Intenzív Terápiás Intézet:https://aok.pte.hu/hu/egyseg/310/index/almenu/83
- Szeged
- Szent Györgyi Albert Klinikai Központ: https://u-szeged.hu/szakk/neur/ambulanciak-rendelesi
- Székesfehérvár
- Fejér Megyei Szent György Kórház: http://www.fmkorhaz.hu/
- Fejérvári Fájdalomterápiás Központ: fájdalom-terápia.hu
- Szekszárd
- Tolna Megyei Balassa János Kórház: http://portal.tmkorhaz.hu/
- Salgótarján
- Szent Lázár Megyei Kórház: http://www.szlmk.hu/
- Szombathely
- Marskusovszky Egyetemi Oktatókórház: http://markusovszky.hu/
- Veszprém
- Csolnoky Ferenc Kórház: http://www.vmkorhaz.hu/korhazweb/index.php
- Zalaegerszeg
- Zala Megei Szent Rafael Kórház: https://www.zmkorhaz.hu
Utánkövetés
NE FELEJTSD EL A RENDSZERES KONTROLLVIZSGÁLATOKAT!
Hospice

A hospice nem arról szól, hogy véget ért az élet, hanem arról, hogy még tart.
Bár a hospice gondozás és a palliatív kezelés célja egyaránt a beteg támogatása és komfortérzetének minél teljesebb kielégítése, a palliatív kezelés már a betegség korábbi szakaszában megkezdődik. A hospice-gondozás a palliatív ellátás azon formája, melyre akkor van szükség, amikor kiderül: a betegség várhatóan rövid időn belül a beteg halálához vezet. Ettől a ponttól a kezelési célok közül kikerül a gyógyítás szándéka, helyét a beteg életminőségének javítása, pszichés vezetése, illetve tüneteinek csillapítása veszi át.
A hospice a súlyos betegségük végstádiumában levő, elsősorban daganatos betegek humánus, összetett ellátását jelenti multidiszciplináris csoport segítségével. Az ellátás célja a betegek életminőségének javítása: testi és lelki szenvedéseik enyhítése, fizikai és szellemi aktivitásuk támogatása, valamint a hozzátartozók segítése a betegség és a gyász terheinek viselésében.
Az ellátásban orvosok, ápolók, gyógytornászok, pszichológusok/mentálhigiénikusok, szociális munkások, lelkészek, dietetikusok és képzett önkéntes segítők vesznek részt. A munkacsoport tagjai így komplex (testi, lelki, szociális, és spirituális) támaszt tudnak nyújtani.
A hospice-ellátás történhet fekvőbeteg intézményekben (szervezetileg önálló hospice-otthonban vagy egy kórház részét képező palliatív osztályon, esetleg kiképzett mobil csoport segítségével, általános osztályokon), ambuláns formában (ún. nappali kórházban), vagy a beteg otthonában (házi szakellátás formájában).
Hospice ellátás formái:
1. intézeti betegellátás: hospice-otthon, hospice palliatív részleg;
2. hospice otthoni szakellátás;
3. átmeneti szervezeti formák: ambuláns gondozás, kórházi konzultatív csoport (mobil team), nappali kórház, gyászcsoport, telefonos segélyszolgálatok.
Az európai hospice alapelvek szerint a hospice ellátás minden formája ingyenes, így valósítható meg a valódi esélyegyenlőség a haldokló ellátásában.
1. Az intézeti hospice ellátás a hospice házakban és a kórházak hospice és palliatív osztályain folyik. Azokra a betegekre irányul, akiknek a tüneteit nem lehet enyhíteni az otthoni körülmények között. Itt olyankor is fogadhatnak betegeket meghatározott időre, amikor tehermentesítő gondozásra van szükség, például amikor a beteg gondozásában kimerült családtagoknak pihenésre van szükségük.
A kórháztól függetlenül működő hospice-otthonba olyan, végstádiumban levő beteg kerül felvételre, aki állapota vagy körülményei miatt otthon nem gondozható, és haláláig ott is marad.
A szanatóriumi körülmények között általában 10–12 beteget helyeznek el, akiknek átlagos ott tartózkodása maximum 3 hónap. A hospice-otthon előnye az otthonos elhelyezés. A kórházban levő hospice-palliatív osztály célja a viszonylag még hosszabb, néhány hónap túlélésre számítható beteg és családtagjai felkészítése az otthoni gondozásra. Az ott tartózkodás alatt beállítják a szükséges fájdalomcsillapító adagot, kezelik a tüneteket, majd a beteget lehetőség szerint otthonába bocsátják. A palliatív osztályon az orvos szerepe meghatározóbb, mint az elsősorban gondozási feladatokat ellátó hospice-otthonban. A betegek elkísérése hosszabb ideig tart, ezért fokozottan szükséges a többi szakember bevonása. Előnyei, hogy az esetleg szükségessé váló kórházi beavatkozások helyben megoldhatók
2. Az otthoni hospice szakellátás jelentősége évről évre növekszik. Az emberek többsége otthon szeretné tölteni utolsó napjait családja körében, de a család általában nem képes vállalni a szakszerű gondozást, segítségre szorul. Ez nemcsak külön személyzetet, hanem segédeszközöket is jelent, amelyet a hazatérő beteg ingyen kap meg használatra. A folyamatos otthoni gondozás megszervezése igen jelentős koordinációs tevékenységet igényel. A szakszemélyzet az orvos útmutatása alapján végzi és ellenőrzi a tünetek kezelését, és többnyire rá hárul a család pszichés támogatása, illetve az edukáció vagyis a család felkészítése, oktatása a gondozási feladatokra. A hospice-otthoni szakellátást – a nem egészségügyi szakfeladatok ellátására – kiegészítheti az önkormányzat gondozási segítsége. Az otthoni ellátás működhet önállóan is, de a legjobban bevált megoldás a hospice-otthonhoz vagy a palliatív osztályhoz való tartozás.
3. Átmeneti szervezeti formák közé tartozik az Ambuláns gondozás, ezeket a fájdalomklinikák, a palliatív és hospice gondozási egységek biztosítják azoknak a betegeknek, akik itt jelentkezni tudnak. Az itt dolgozó szakemberek szükség szerint módosítják a fájdalomcsillapító adagot, gyógytornász, pszichológus, foglalkozás-terapeuta is foglalkozik a beteggel.
Ehhez a csoporthoz tartoznak a kórházi konzultatív csoportok vagyis a mobil teamek. Az alapellátást a betegek megkapják az adott osztály személyzetétől, a mobil team a fájdalomcsillapítással és tüneti kezeléssel kapcsolatos speciális feladatokat végzi. Ezek a csoportok konzultatív és oktató szerepet is betöltenek az egészségügyi intézményekben. A mobil team előnyei, hogy a betegek is sokszor szívesebben maradnak a megszokott kórházi osztályukon, és pozitív hatással van a kórházi személyzet attitűdjére.
Nappali kórház (szanatórium) is egy átmeneti forma, amely nappali ellátást nyújtó központok azon betegek számára, akik otthon tartózkodnak, de bizonyos időszakokra képesek otthonukat elhagyni. A nappali központokban való tartózkodás az ottani hangulatnak, foglalkozásoknak és kezeléseknek köszönhetően javítja a betegek életminőségét, ugyanakkor tehermentesíti a családot – biztosítva számukra a pihenést.
Fontos beszélni a gyászolókat támogató csoportokról is, melyek azoknak nyújtanak segítséget, akik nehezen tudnak megbirkózni a közeli hozzátartozó elvesztésével, illetve szívesen találkoznak „sorstársaikkal”, hogy megosszák tapasztalataikat, gondjaikat. Ezek az egységek az otthoni hospice szolgálattal, a hospice-otthonnal vagy a palliatív osztállyal állnak kapcsolatban. Átmeneti szervezeti formákhoz tartoznak még a telefonos segélyszolgálatok, akik az előrehaladott állapotú betegeket ellátó szakembereknek és hozzátartozóknak adnak tanácsot, és lehetőséget nyújtanak a különböző egészségügyi szolgálatoknak, hogy palliatív szakellátó egységekkel, mobil teamekkel vagy intézeti részlegekkel lépjenek kapcsolatba.
A hospice szolgálattal való kapcsolatfelvétel nem lemondást jelent az életről, hanem az egyik a legfontosabb dolog, amit a beteg önmagáért vagy a hozzátartozó a betegért megtehet.
Szószedet
Adjuváns terápia - Olyan gyógykezelés, amit az első kezelés után írnak elő, azért, hogy csökkentsék a rák kiújulásának kockázatát.
Anesztézia - Vizsgálatok és sebészeti beavatkozások alatti gyógyszeres ellátás bizonyos testrészek érzéstelenítésére. Ilyen az altatás is.
Áttét - A rák átterjedése a szervezet egyik részéből a másikba.
Beleegyező nyilatkozat – Az az eljárás, amely során a páciens a betegséggel kapcsolatos minden fontos információt megkap, beleértve az eljárással, teszttel, kezeléssel kapcsolatos előnyöket és hátrányokat is, annak eldöntésére, hogy hozzájárul-e a kezeléshez, teszthez, illetve részt kíván-e venni klinikai vizsgálatban.
Biomarker - Gének, fehérjék és egyéb anyagok, amelyek információt szolgáltatnak a daganattal kapcsolatban. Minden egyes daganat egyedi biomarkerek együttesével rendelkezik, amelyek kimutathatóak testnedvekből vagy szövetekből. Ezek segíthetnek a megfelelő kezelés kiválasztásában.
Biopszia - Szövet egy kis részének sebészeti eltávolítása mikroszkóp alatti vizsgálat céljából, hogy el lehessen dönteni, fennáll-e a betegség.
Borderline-típusú petefészekrák - Olyan típusú daganat, amely lassan nő, és általában nem ad áttétet, ami azt jelenti, hogy az eltávolító műtét után csekély a kiújulás esélye.
BRCA1 és BRCA2 - Olyan gének, amelyek normális esetben védelmet nyújtanak a petefészekrák ellen azáltal, hogy segítenek megjavítani a sérült sejteket, amelyek daganatos betegséget okozhatnak, de növelhetik a daganat kialakulásának esélyét, ha megváltoznak vagy mutálódnak. Az emberek örökölhetik ezeket a megváltozott vagy mutálódott géneket a szüleiktől.
CA125 - Egyes petefészekrák-sejtek által termelt fehérje. A CA125 magas szintje a vérben petefészekrákra utalhat. A ‘CA’ a Rák Antigén (Cancer Antigen) rövidítése.
Célzott terápia - Olyan kezelés, amely konkrét daganatos sejteket céloz. Ezeknek az eljárásoknak általában kevesebb mellékhatásuk van, mint a hagyományos kemoterápiás kezeléseknek.
Ciszta - Egy kis szövetdarab, ami bárhol kialakulhat a testben. Folyadékkal, levegővel, gennyel vagy egyéb anyaggal lehet tele. A legtöbb ciszta nem rákos.
Citoreduktív műtét - Olyan műtét, ahol megpróbálnak annyit eltávolítani a daganatból, amennyit csak lehetséges.
CT vizsgálat - Olyan vizsgálat, ahol röntgensugárral és számítógéppel készítenek képeket a test belsejéről.
Daganat/rák - Gyűjtőfogalom olyan betegségekre, amelyek esetében a kóros sejtek kontroll nélkül osztódnak, behatolnak a közeli szövetekbe, és átterjednek a test egyéb részeire is.
Elsődleges kezelés - Az első kezelés, amit egy betegség kezelése során alkalmaznak. Más néven elsődleges terápia vagy elsővonalbeli kezelés.
Epitheliális (hámeredetű) petefészekrák - Olyan daganatfajta, amelynél a rák a petefészek felszínén lévő sejtekben van.
Genetika - A gének tanulmányozásának tudománya.
Gének - A DNS kis részei, amelyek olyan információkat hordoznak, amelyek meghatározzák azokat az egyéni tulajdonságokat, jellemzőket, amelyek szülőkről gyerekekre öröklődnek.
Germ cell (rosszindulatú csírasejtes) petefészekrák - Olyan daganattípus, amely a petefészek csírasejtjeiből indul ki (petefészek sejtjei, amelyek petesejtté fejlődnek).
Has - A test azon része, ami magában foglalja a gyomrot, a beleket és más emésztőszerveket.
Hashártya - A hasfalat borító szövet, amely a hasüregben található szervek nagy részét is fedi.
Homológ rekombinációs deficiencia tesztelése - A daganatból műtét vagy biopszia során mintát vesznek. Ha a HRD-vizsgálat eredménye pozitív, akkor valószínűbb, hogy bizonyos kezelési módszerek, mint például a PARP-gátlás, hatásosak lesznek.
Hormonok - Az emberi testben természetesen előforduló anyagok, amelyek a véráramban keringenek, és bizonyos sejtek vagy szervek működését szabályozzák.
Hormonpótló terápia - Szintetikus hormonokkal (ösztrogén, progeszteron vagy mindkettő) folytatott kezelés, amelyeket menopauza után adnak a petefészek által már nem termelt hormonok pótlására.
Hormonterápia - Egyfajta kezelés, amely hormonokat ad hozzá, blokkol vagy épp kivon a szervezetből, bizonyos ráktípusok növekedésének lassítása vagy megállítása érdekében.
Hospice - Egy olyan egészségügyi ellátás, amely inkább a fájdalom csillapítására koncentrál, ha a gyógyítás már nem lehetséges.
Hysterectomia - A méh műtéti eltávolítása.
Immunterápia - Olyan típusú gyógyszeres eljárás, amely a test immunrendszerét hívja segítségül a daganatos és egyéb betegségek leküzdéséhez.
Infúzió - Egy olyan eljárás, amely során lassan, a vénán keresztül közvetlenül a véráramba folyadékot, leggyakrabban gyógyszert tartalmazó folyadékot juttatnak. Intravénás infúziónak is nevezik.
Inoperábilis – Annak a daganatnak a leírására használják, amely műtéttel nem távolítható el.
Intraperitoneális - A peritoneális üregen belüli (a test azon része, amely a hasi szerveket tartalmazza).
Intravénás - Gyógyszer bevitele a vénába fecskendezve, vagy infúzió által.
Jóindulatú - Olyan daganattípusok, amelyek nem veszélyesek, és amelyek az eltávolítás után nem újulnak ki.
Karcinóma - A rákos elváltozás másik neve. A szervek belsejéből vagy azok külső rétegéből indul.
Kemoterápia - A rákos sejtek leküzdésére és elpusztítására szolgáló gyógyszerek alkalmazása. A gyógyszerek megakadályozzák a rákos sejtek szaporodását, ami segít meggátolni azok növekedését és a testben való szétterjedését.
Kiújulás - Amikor a rák egy idő után, amikor nem lehetett kimutatni, visszatér.
Klinikai vizsgálat - Kutatás, melyben azt tesztelik, hogy az új gyógyszerek és kezelési eljárások működnek-e.
Laparoszkóp - A has belső vizsgálatára szolgáló műszer, amellyel a laparoszkópiát végzik.
Laparoszkópia - Annak az eljárásnak a neve, amely során a laparoszkóp segítségével elvégzik a has vizsgálatát. Nem vágják fel a hasat, hanem néhány ponton/lyukon keresztül jutnak belülre a műszerrel.
Medence - A has alsó része, amely a csípőcsontok között helyezkedik el.
Menopauza - Az az időszak a nők életében, amikor a petefészkekben leáll a hormontermelés, és ezzel együtt elmarad a menstruáció.
Méh - Női reprodukciós szerv, ahol a magzat (meg nem született baba) kihordásra kerül.
Méhnyak - Keskeny járat, amely a hüvely felső részén található, és amely a méh alsó részét képezi.
Méhnyálkahártya - Vékony szövetréteg, amely a méhet béleli.
MR/MRI (mágneses rezonanciás képalkotó vizsgálat) - Olyan orvosi képalkotási technika, amely egy mágneses mezőt, és számítógép által generált rádióhullámokat használ a test szerveit és szöveteit ábrázoló, részletes felvételek elkészítéséhez. Az MRI vizsgálatnál nincs káros sugárzás.
Neoadjuváns terápia - Olyan kezelés, amely az első lépés lehet a daganat méretének csökkentésére a fő kezelés megkezdése előtt. Ilyen például a kemoterápia, a sugár- vagy hormonkezelés.
Nőgyógyászati daganat - A női reproduktív rendszert érintő daganatos betegségek, melybe beletartozik a méhnyak, a méhnyálkahártya, a petevezetékek, a petefészkek, a méhtest és a hüvely rákos megbetegedése.
Nőgyógyász-onkológus - A női reproduktív rendszer daganatos megbetegedéseinek kezelésére szakosodott orvos.
Nyirokcsomók - Kis kör alakú szervek, melyek a test immunrendszerének részei. Fehérvérsejteket tartalmaznak, amelyek segítenek a szervezetnek legyőzni a fertőzéseket, betegségeket.
Onkológus - A rák kezelésére specializálódott orvos.
Oophorectomia - Olyan műtéti eljárás, amely során az egyik vagy mindkét petefészek eltávolításra kerül.
Palliatív ellátás - Olyan ellátási mód, ahol elsősorban nem a gyógyítás, hanem a tünetek enyhítése a cél, olyan súlyos betegségek esetén, mint például a rák.
PARP-gátló - Egy olyan célzott gyógyszer a rák ellen, amely megakadályozza, hogy a rákos sejtek saját magukat javítani tudják, így aztán elhalnak.
Petefészek - Páros női nemi szerv, amelyben a peték termelődnek, tárolódnak, majd kilökődnek.
Petefészekrák - Olyan daganatos betegség, amely a petefészek szöveteiben keletkezik.
Petevezetékek - Azok a vezetékek, amelyek lehetővé teszik a petesejt számára, hogy a petefészekből a méhbe jusson.
Placebo - Egy inaktív anyag neve (amelyet úgy fejlesztettek, hogy ne legyen terápiás értéke), ami pontosan úgy néz ki, mint egy olyan gyógyszer, amit egy klinikai vizsgálat során tesztelnek. Az aktív gyógyszer hatását a placebo hatásával vetik össze.
Prognózis - Egy betegségnek - mint például a rák - a lehetséges kimenetele (túlélési esély).
Refraktált - Olyan betegség vagy állapot leírására szolgál, ami nem reagál a kezelésre.
Remisszió - Egy időszakot jelző fogalom, amikor a rák jelei és tünetei csökkenek vagy teljesen eltűnnek.
Rosszindulatú - Egy alternatív kifejezés a rákos elváltozásra.
Rosszindulatú áttét - Amikor a rák átterjed a test egyik részéből a másikba.
Salpingo-oophorectomia - Olyan műtét, melynek során eltávolításra kerülnek a petefészkek és a petevezetékek.
Salpingectomia - Olyan műtét, melynek során eltávolításra kerülnek a petevezetékek.
Sejtek - Minden élőlény mikroszkopikus építőelemei.
Stabil állapot - Amikor a daganat mérete nem növekszik, és nem is csökken.
Stádiumbesorolás - Vizsgálatok és tesztek elvégzése annak megállapítására, hogy mekkora a daganat, és milyen messze terjedhetett attól a ponttól, ahonnan kiindult.
Stromális petefészekrák - Olyan daganatok, melyek a petefészek kötőszöveti sejtjeiben fejlődnek ki.
Sugárterápia - Olyan kezelési eljárás, ami nagy energiájú sugárzást alkalmaz a rákos sejtek elpusztítására, és a daganat méretének csökkentésére.
Szövettan - Szövetek és sejtek mikroszkópos vizsgálata.
Tumor - Egy csomó vagy sejtcsoport, amely akkor képződik, amikor a sejtek a normálistól eltérően nőnek és osztódnak. A daganat lehet rákos (rosszindulatú) vagy jóindulatú.
Ultrahang - Olyan vizsgálat, ami egy hasi detektoron keresztül, hanghullámok segítségével képeket alkot a testben lévő szervekről. Az ultrahangos vizsgálat nem használ káros sugárzást.
Felhasznált források
http://otszonline.hu/cikk/lathataron_egy_ujabb_parp_inhibitor_petefeszekrakra
https://pubmed.ncbi.nlm.nih.gov/26177554/
Nőgyógyászati Onkológia, Gyakorlati kézikönyv, dr. Pete Imre- dr. Kásler Miklós, 2012.
Emlő-és nőgyógyászati onkológia, Bodoky György, Kopper László, 2012.
A szülészet-nőgyógyászat tankönyve, Papp Zoltán, 2009.
MályvaZseb, HPV és minden, ami még belefért, Tóth-Lukács, 2020.
daganatok.hu
intima.hu
futureproofinghealthcare.com
ESGO Guidlines, Cervical cancer Pocket Guidlines
klivi.hu
tajekozottbeteg.hu
noidaganatok.hu
ESMO pocket guidline, Gynaecological malignancies, 2018.
https://www.uchicagomedicine.org/cancer/types-treatments/hipec








